Катализаторы играют важную роль в различных химических реакциях, прежде всего, ускоряя их скорость. Однако, влияют ли они на константу равновесия? Вопрос, безусловно, вызывает интерес ученых и студентов, поскольку понимание этого явления может иметь значительное значение для практического применения катализаторов и дальнейшего развития химии.
Чтобы ответить на этот вопрос, необходимо вначале разобраться в сущности константы равновесия. Константа равновесия представляет собой множитель, который характеризует соотношение концентраций реагентов и продуктов в химической реакции на ее равновесном состоянии при постоянной температуре и давлении. Константа равновесия является постоянной для конкретной реакции и может характеризовать скорость ее протекания.
На первый взгляд казалось бы, что катализаторы никак не влияют на константу равновесия, так как они не участвуют в окончательной стадии реакции и остаются неизменными в конце процесса. Однако, современные исследования показывают, что катализаторы могут влиять на равновесие, изменяя скорость продукции или потребления реагентов.
Зависимость константы равновесия от катализатора

Катализаторы играют важную роль в химических реакциях, влияя на их скорость и константу равновесия. Константа равновесия (K) определяет, в какой степени реакция проходит в прямом или обратном направлении при достижении равновесия.
В обычных условиях, константа равновесия не зависит от катализатора, поскольку он не входит в окончательные химические уравнения реакции. Однако, катализаторы могут влиять на скорость достижения равновесия, что может изменить время, необходимое для установления равновесия
Катализаторы обычно снижают активационную энергию реакции, что позволяет молекулам входить в промежуточные состояния и образовывать продукты реакции. Это позволяет ускорить химическую реакцию и сократить время, необходимое для достижения равновесия.
Также, катализаторы могут изменять состав равновесной смеси, поскольку они могут влиять на скорость прямой и обратной реакций. Это может привести к смещению равновесия в определенном направлении и изменению константы равновесия.
Влияние катализатора на константу равновесия
Константа равновесия (K) определяет соотношение концентраций реагентов и продуктов в равновесном состоянии. Математически она определяется как отношение произведения концентраций продуктов к произведению концентраций реагентов, каждое взятое согласно их стехиометрическим коэффициентам в уравнении реакции:
K = ([C]продуктыa[D]продуктыb)/([A]реагентыc[B]реагентыd)
Когда константа равновесия больше единицы, это означает, что продукты более стабильны по сравнению с реагентами и реакция смещается вправо в направлении продуктов. Когда константа равновесия меньше единицы, происходит смещение реакции влево в направлении реагентов.
Влияние катализатора на константу равновесия может быть связано с несколькими факторами:
- Ускорение скорости прямой и обратной реакции. Катализатор может ускорить и прямую, и обратную реакцию, не меняя при этом константу равновесия. Это связано с тем, что обе стороны реакции ускоряются в одинаковой степени, что позволяет сохранить исходное соотношение концентраций реагентов и продуктов.
- Изменение активации реакции. Катализатор может изменить энергию активации для прямой и обратной реакций, что влияет на скорость перехода между состояниями реагентов и продуктов. Это может привести к изменению константы равновесия, поскольку скорость прямой и обратной реакции становятся несоответствующими. В результате реакция может сместиться в одну из сторон для достижения нового равновесного состояния.
- Изменение реакционных механизмов. Катализатор может изменить механизм реакции, что также может привести к изменению константы равновесия. Изменение реакционного механизма может привести к образованию новых промежуточных или сторонних продуктов, которые могут влиять на концентрации реагентов и продуктов.
В целом, влияние катализатора на константу равновесия зависит от специфики реакции и свойств катализатора. Оно может быть сложным и требовать проведения дополнительных экспериментов для полного понимания механизма и его влияния на равновесие реакции.
Катализаторы и скорость химической реакции

Катализаторы играют важную роль в химических реакциях, влияя на их скорость. Скорость химической реакции определяется частотой столкновений между реагирующими частицами и энергией, необходимой для преодоления активационного барьера. Катализаторы влияют на эту энергию активации, снижая ее значение.
Катализаторы могут быть гомогенными, когда они находятся в одной фазе с реагентами, или гетерогенными, когда они находятся в разных фазах. Гомогенные катализаторы обычно растворены в реагенте, в то время как гетерогенные катализаторы представлены в виде поверхности, на которую могут адсорбироваться реагенты.
Катализаторы увеличивают скорость химической реакции, обеспечивая альтернативные пути реакции с меньшей энергией активации. Они участвуют в реакции, образуя промежуточные комплексы с реагентами, что способствует образованию конечного продукта.
В зависимости от механизма действия катализаторов, они могут быть классифицированы как ферменты, гетерогенные и гомогенные катализаторы. Ферменты - это биологические катализаторы, специфически связанные с определенными реакциями в организме. Гетерогенные катализаторы активны при контакте с реагентами на своей поверхности, в то время как гомогенные катализаторы растворены в реакционной среде.
Влияние катализаторов на константу равновесия химической реакции незначительно. Константа равновесия определяется распределением реагентов и продуктов между различными фазами системы, а катализаторы обычно не влияют на это распределение. Константа равновесия является характеристикой системы в стационарном состоянии и зависит от температуры и начального состояния системы, но не зависит от наличия катализаторов.
| Тип катализатора | Принцип действия |
|---|---|
| Ферменты | Ускорение реакций в организме путем связывания с реактантами и образования промежуточных комплексов |
| Гомогенные катализаторы | Растворены в реакционной среде и участвуют в реакции, образуя промежуточные комплексы |
| Гетерогенные катализаторы | Активны на своей поверхности и взаимодействуют с реагентами, образуя промежуточные комплексы |
Таким образом, хотя катализаторы могут влиять на скорость химической реакции, они обычно не влияют на константу равновесия реакции. Их влияние связано с образованием промежуточных комплексов и облегчением прохождения активационного барьера, что приводит к повышению скорости реакции, но не изменяет соотношение между реагентами и продуктами в равновесной системе.
Роль катализатора в смещении равновесия
Катализаторы играют важную роль в химических реакциях, в том числе в смещении равновесия. Они могут значительно повлиять на скорость и направление реакции, хотя сама константа равновесия не зависит от присутствия катализатора.
Катализаторы предоставляют новые пути реакции, снижая энергетический барьер и ускоряя химические превращения. Они влияют на скорость и направление реакции, но не меняют начальные и конечные состояния системы. Таким образом, катализаторы не влияют на константу равновесия, которая определяет соотношение концентраций реагентов и продуктов в состоянии равновесия.
Однако, с использованием катализатора можно изменить время, необходимое для достижения равновесия. Он ускоряет обратную и прямую реакции одновременно, сохраняя равновесное состояние системы. Катализаторы облегчают переходную стадию реакции, снижая активационную энергию, что увеличивает скорость достижения равновесия.
Таким образом, катализаторы играют важную роль в химических системах, увеличивая скорость реакции и сокращая время до достижения равновесия. Но они не влияют на саму константу равновесия, которая остается постоянной при тех же условиях.
Механизмы взаимодействия катализатора с реагентами
Катализаторы играют важную роль в химических реакциях, ускоряя их скорость и снижая активационную энергию. В зависимости от типа реакции и катализатора механизмы их взаимодействия могут различаться.
Одним из основных механизмов взаимодействия катализатора с реагентами является адсорбция. Катализатор может адсорбировать реагенты на своей поверхности, образуя активные центры. Это позволяет реагентам более эффективно взаимодействовать и проходить реакцию с нижней энергией активации.
Другим механизмом взаимодействия катализатора с реагентами является координационная активация. Катализатор может образовывать координационные связи с реагентами, что увеличивает вероятность правильного взаимодействия и образования промежуточных соединений.
Также, катализаторы могут проводить протонную или электронную передачу между реагентами, участвуя в образовании или разрыве химических связей. Это может изменять энергетический профиль реакции и способствовать образованию продуктов более высокой энергии.
Кроме того, некоторые катализаторы могут создавать определенные условия реакции, например, обеспечивать оптимальную температуру или pH-уровень. Это также может влиять на скорость и селективность реакции.
Таким образом, механизмы взаимодействия катализатора с реагентами могут быть разнообразными и зависят от конкретной реакции и типа катализатора. Изучение этих механизмов позволяет более глубоко понять процессы, протекающие в химической реакции, и оптимизировать условия ее проведения.
Типы катализаторов и их влияние на константу равновесия
В зависимости от своего состава и механизма действия, катализаторы могут быть классифицированы на следующие типы:
| Тип катализатора | Описание | Примеры |
|---|---|---|
| Гомогенные катализаторы | Реагенты, которые растворяются в реакционной среде и действуют в реакционной среде одинаково со всеми частицами. | Кислоты, основания, металлосоединения |
| Гетерогенные катализаторы | Катализаторы, которые существуют в одной фазе со смесью реагентов, но имеют разные свойства и химическую активность. | Металлы, оксиды, полимеры |
| Ферменты | Биологические катализаторы, состоящие из белков и участвующие в метаболических реакциях. | Амилаза, липаза, ДНК-полимераза |
Влияние катализатора на константу равновесия реакции зависит от его характера и механизма действия. Гомогенные катализаторы обычно не влияют на значение константы равновесия, так как они участвуют в реакции одинаково с обоими обратными реагентами. Однако, они могут повысить скорость достижения равновесного состояния.
Гетерогенные катализаторы могут влиять на константу равновесия, так как они вступают в реакцию только с одним из обратных реагентов. При наличии гетерогенного катализатора, константа равновесия может измениться в направлении, увеличивающем количество продукта или реагента в равновесной смеси.
Ферменты, в качестве гомогенных биокатализаторов, обладают специфичностью действия и могут значительно повлиять на константу равновесия в биологических системах. Они способны ускорять реакции, обратные которым обычно протекают очень медленно.
Таким образом, тип катализатора и его свойства определяют его влияние на константу равновесия. Использование катализаторов может быть эффективным способом изменения равновесной смеси в химических и биологических реакциях.
Эффективность различных типов катализаторов
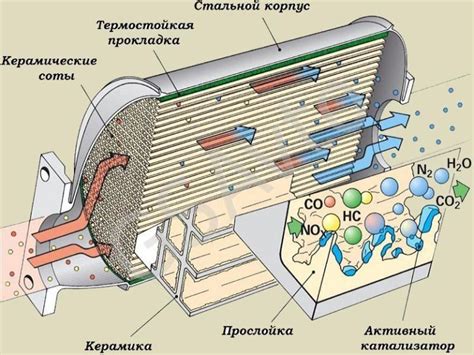
Одним из наиболее распространенных типов катализаторов являются металлические катализаторы, такие как платина, никель или железо. Они обладают высокой активностью и часто используются в промышленности. Однако, их эффективность может зависеть от условий реакции, таких как температура и давление.
Помимо металлических катализаторов, существуют также гетерогенные и гомогенные катализаторы. Гетерогенные катализаторы находятся в разных фазах с реагентами и обычно представляют собой твердые поверхности, такие как оксиды металлов или зеолиты. Они имеют большую площадь поверхности и обладают высокой стабильностью. Гомогенные катализаторы, напротив, находятся в одной фазе с реагентами и растворены в реакционной среде, в основном вода или органические растворители.
Кроме того, катализаторы могут быть различными по химической природе. Например, существуют кислотные и щелочные катализаторы, которые активизируют реакцию путем донорно-акцепторных взаимодействий с реактивами. Также существуют энзимные катализаторы, такие как ферменты, которые играют важную роль в биологических процессах.
Важно отметить, что эффективность катализаторов может зависеть от самой реакции. Одни катализаторы могут быть более эффективными в одних реакциях, нежели в других. Например, катализатор, эффективный в одной реакции равновесия, может быть неэффективен в другой из-за разницы в механизмах реакции или условиях.
Таким образом, эффективность катализаторов влияет на константу равновесия. Выбор катализатора является важным шагом в разработке каталитических процессов, и требует учета различных факторов, таких как тип реакции, условия и химическая природа катализатора.
Применение катализаторов в промышленности
Одним из наиболее распространенных применений катализаторов в промышленности является процесс производства аммиака. Применение катализатора, обычно состоящего из металлической сетки покрытой специальным материалом, позволяет значительно увеличить скорость реакции образования аммиака из азота и водорода. Благодаря этому процесс производства аммиака становится более эффективным и экономически выгодным.
Другим примером применения катализаторов является процесс гидроочистки нефти. В процессе гидроочистки нефтепродуктов из них удаляются различные примеси и загрязнения, что позволяет получить более чистый и качественный продукт. Применение катализаторов в этом процессе позволяет значительно ускорить реакцию и повысить степень очистки нефти.
Катализаторы также широко используются в процессах синтеза органических соединений, производства пластмасс, производства удобрений и многих других отраслях промышленности. Их применение позволяет получить высокую эффективность процесса, снизить затраты на производство и улучшить качество продукции.
Таким образом, катализаторы играют важную роль в промышленности, повышая эффективность процессов и снижая их затраты. Применение катализаторов является ключевым фактором для развития и совершенствования промышленных процессов, а также ведет к улучшению экологической ситуации и снижению негативного влияния на окружающую среду.
Плюсы и минусы использования катализаторов в химических реакциях

Плюсы использования катализаторов:
- Ускорение реакции: Главное преимущество катализаторов заключается в их способности ускорить химическую реакцию. Благодаря катализатору, реакция может протекать при более низких температурах и с меньшим количеством энергии, что экономит время и ресурсы.
- Повышение эффективности: Использование катализаторов позволяет достичь более высокой степени превращения и выхода продукта, что способствует повышению эффективности химического процесса.
- Выборочная активация: Катализаторы могут обладать способностью проводить выборочную активацию определенных реагентов, что позволяет получать определенные продукты реакции.
- Снижение побочных продуктов: В некоторых случаях катализаторы могут снижать образование побочных продуктов, что положительно сказывается на экологической стороне химических процессов.
- Возможность повторного использования: Катализаторы могут быть использованы неоднократно, что уменьшает затраты на производство и повышает экономическую эффективность.
Минусы использования катализаторов:
- Выбор катализатора: Выбор подходящего катализатора для определенной реакции может быть сложным и требовать тщательного подбора.
- Длительность исследований: Разработка новых катализаторов требует проведения множества экспериментов и исследований, что может занимать значительное время и ресурсы.
- Деактивация: Катализаторы могут подвергаться деактивации, что приводит к снижению их эффективности и требует проведения процессов реактивации или замены.
- Токсичность: Некоторые катализаторы могут быть токсичными или опасными для окружающей среды, что требует соблюдения специальных мер предосторожности при их использовании и утилизации.
Способы оптимизации катализаторов для повышения константы равновесия
Улучшение катализаторов можно достичь различными способами:
1. Изменение структуры и состава катализатора. Путем внесения определенных изменений в структуру и состав катализатора можно достичь повышения его эффективности. Например, можно изменить поверхность катализатора, введя новые активные центры, повышающие скорость реакции.
2. Модификация поверхности катализатора. С помощью модификации поверхности катализатора можно изменить его химическую активность и селективность. Например, можно нанести на поверхность катализатора металлические или оксидные добавки, которые улучшат его каталитические свойства.
3. Оптимизация размера и формы частиц катализатора. Размер и форма частиц катализатора имеют большое значение для его активности и стабильности. Оптимальный размер частицы катализатора может обеспечить максимальную доступность активных центров и повысить скорость реакции.
4. Введение подходящих промежуточных поглотителей. Применение подходящих промежуточных поглотителей может стабилизировать катализатор и улучшить его селективность. Например, введение молекулярного кислорода может увеличить эффективность окислительных реакций.
Все эти методы оптимизации катализаторов позволяют повысить константу равновесия реакции, что способствует увеличению выхода целевых продуктов и снижению затрат на процесс. Таким образом, исследование и разработка новых способов оптимизации катализаторов играют важную роль в современной химической промышленности.
Новые тенденции в разработке катализаторов

Катализаторы играют важную роль в химических реакциях, ускоряя и усиливая процессы синтеза и превращения. Недавние исследования показали, что выбор катализатора может существенно влиять на константу равновесия химической реакции.
Современные исследования в области катализа сфокусированы на разработке новых материалов с улучшенными каталитическими свойствами. Одним из направлений является создание катализаторов с высокой активностью и стабильностью. Учитывая, что выбор катализатора может оказывать влияние на константу равновесия, разработка новых материалов позволяет улучшить эффективность и рентабельность процессов.
Важным аспектом при разработке катализаторов является выбор оптимального типа активного центра и его структурных характеристик. Исследования в области нанокатализа позволяют создавать структуры с определенными размерами и формами, что существенно влияет на их каталитическую активность. Например, наночастицы металлов могут обладать значительно большей активностью по сравнению с их более крупными аналогами. Эти новые технологии открывают новые горизонты в области синтеза и превращения веществ.
Также, в последние годы исследователи обратили свое внимание на разработку экологически чистых катализаторов, которые были бы более устойчивыми к деградации и обладали меньшими негативными экологическими последствиями. Например, разработка наноструктур с использованием экологически чистых материалов, таких как зеленая химия, может привести к созданию новых катализаторов с высокой активностью и стабильностью, не требующих использования опасных веществ.
Сложная структура катализаторов представляет собой интересную область для исследования и оптимизации. Моделирование и экспериментальные методы позволяют изучать и оптимизировать различные аспекты, такие как форма, размер и состав катализатора. Таким образом, новые тенденции в разработке катализаторов объединяют современные методы синтеза и анализа с инновационными стратегиями по улучшению эффективности катализа.
- Разработка новых материалов с улучшенными каталитическими свойствами
- Выбор оптимального типа активного центра и его структурных характеристик
- Исследования в области нанокатализа
- Разработка экологически чистых катализаторов
- Моделирование и оптимизация структуры катализаторов
Новые тенденции в разработке катализаторов открывают новые перспективы для контроля химических реакций и повышения их эффективности. Дальнейшие исследования в этой области могут привести к созданию более эффективных и устойчивых катализаторов, что будет способствовать развитию различных отраслей промышленности и научных открытий.




