Метан - одно из наиболее распространенных органических соединений, которое играет важную роль в природе. Однако, мало кто задумывается о том, почему именно молекула метана обладает такой особенной формой - тетраэдрической. В этой статье мы рассмотрим причины, по которым молекула метана имеет именно такую структуру.
Первой причиной является способность атомов водорода образовывать только одну ковалентную связь. Каждый атом водорода может вступать только в одну связь с другим атомом. Из-за этого, молекула метана, состоящая из четырех атомов водорода и одного атома углерода, формирует строго определенную тетраэдрическую структуру. Каждый атом водорода связан с атомом углерода, образуя углы в 109,5 градусов между собой.
Второй причиной является то, что молекула метана стремится к наиболее устойчивому состоянию. Тетраэдрическое строение молекулы метана является наиболее энергетически выгодным и устойчивым. Угол между атомами водорода также обеспечивает максимальное равновесие и минимальное отталкивание между ними, что делает молекулу метана очень стабильной и надежной.
Таким образом, молекула метана имеет тетраэдрическое строение из-за особенностей химической связи между атомами водорода и углерода, а также из-за стремления к наиболее стабильному состоянию. Эти факторы определяют форму и свойства молекулы метана, которые играют важную роль в ее химической и физической активности.
Метан: тетраэдрическое строение молекулы и его обусловленность
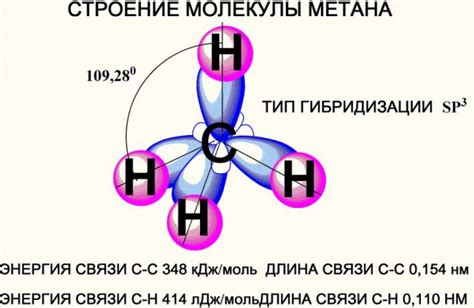
- Расположение атомов. В молекуле метана атом углерода находится в центре, а атомы водорода расположены симметрично вокруг него. Это приводит к образованию структуры, напоминающей тетраэдр.
- Сп^3-гибридизация углерода. Молекула метана образуется в результате гибридизации одного s-орбиталя и трех p-орбиталей углерода. Это приводит к образованию четырех sp^3-гибридных орбиталей, на каждой из которых находится пара электронов.
- Электронная геометрия. Тетраэдрическое строение молекулы метана связано с такой электронной геометрией, как сп^3-гибридизация. Эта геометрия обусловлена стремлением молекулы минимизировать отталкивания между парами электронов, находящихся на sp^3-гибридных орбиталях углерода.
Тетраэдрическое строение молекулы метана также оказывает влияние на его физические и химические свойства. Благодаря расположению атомов в пространстве и электронной геометрии, метан является неполярной молекулой, не образуются диполь-дипольные взаимодействия. Это делает его безцветным, без запаха и слабо растворимым в воде.
Метан как самый простой углеводород
Строение метана является тетраэдрическим, то есть атом углерода находится в центре молекулы, а четыре атома водорода располагаются вокруг него, образуя углы равные примерно 109,5 градусов между собой. Такое строение обусловлено электронной структурой атомов углерода и водорода, где они стремятся к заполнению своих валентных энергетических оболочек.
Углеродный атом в метане обладает четырьмя электронными парами, каждая из которых образует химическую связь с одним атомом водорода. Такое строение обеспечивает метану высокую устойчивость и стабильность, а также способность образовывать различные химические соединения и участвовать в реакциях с другими веществами.
| Формула | Название | Количество атомов углерода |
|---|---|---|
| CH4 | Метан | 1 |
| C2H6 | Этан | 2 |
| C3H8 | Пропан | 3 |
| C4H10 | Бутан | 4 |
| C5H12 | Пентан | 5 |
Метан широко используется как источник энергии, особенно в горючих газах и топливах. Он также служит главным ингредиентом при производстве ацетилена и других органических соединений. Кроме того, метан играет важную роль в биологических процессах, таких как переваривание и брожение в желудках рогатого скота и других животных.
Таким образом, метан как самый простой углеводород имеет тетраэдрическое строение, которое обеспечивает ему устойчивость и способность к различным химическим реакциям. Его широкое использование и наличие в атмосфере делают его важным газом для изучения и понимания многих аспектов природы и жизни на Земле.
Тетраэдрическое строение молекулы метана
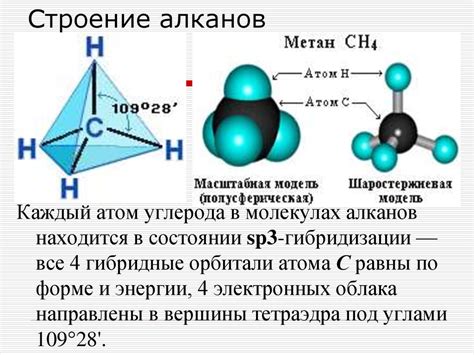
Тетраэдрическая форма молекулы метана означает, что каждый атом водорода равноудален от атома углерода, образуя равносторонний тетраэдр. Это означает, что углеродный атом находится в центре тетраэдра, а атомы водорода равномерно распределены вокруг него.
Форма тетраэдра достигается благодаря трем основным факторам: геометрии углеродного атома, образованию связей с атомами водорода и электронной структуре молекулы метана. Углеродный атом в метане обладает сп3-гибридным состоянием, что означает, что он образует четыре одинаковые связи с атомами водорода, изменяя свою геометрию с плоской к сплюснутой тетраэдрической.
Тетраэдрическое строение молекулы метана является одной из основных причин его стабильности и низкой реакционной активности. Это также защищает метан от воздействия внешних условий и обеспечивает ему множество применений, включая использование в качестве источника энергии и сырья для производства различных химических соединений.
Факторы, определяющие тетраэдрическое строение молекулы метана
Тетраэдрическое строение молекулы метана определяется несколькими факторами:
| Фактор | Объяснение |
|---|---|
| Геометрия атомов | Углерод является атомом со сп^3-гибридизацией, что позволяет ему образовывать четыре одинаковые σ-связи с атомами водорода. Такая гибридизация обеспечивает наиболее энергетически выгодное расположение атомов и минимизирует отталкивание между ними. |
| Пространственная симметрия | Тетраэдрическая структура метана обладает высокой симметрией, что позволяет максимально эффективно распределить отталкивающие силы между четырьмя атомами водорода. Такое расположение атомов минимизирует энергию системы и делает молекулу стабильной. |
| Распределение электронной плотности | Электронная плотность в молекуле метана равномерно распределена между атомами углерода и водорода. Это связано с симметричным расположением атомов и эффективным взаимодействием с электронами. |
Тетраэдрическое строение молекулы метана имеет значительное значение для его химических свойств и реакций. Оно определяет геометрическую форму молекулы, взаимодействие с другими молекулами и возможность образования связей с другими атомами.




