Мыло – один из наиболее распространенных моющих средств, используемых в повседневной жизни. Оно широко применяется для очистки различных поверхностей, будь то посуда, тело или предметы в домашнем хозяйстве. Но почему именно мыло так эффективно удаляет грязь? Научные исследования показывают, что причина кроется в особой структуре и химических свойствах мыла.
Основным компонентом мыла являются молекулы, которые называются поверхностно-активными веществами. Они состоят из двух частей: «фильмообразующей» головки и «вытянутого» хвостовика. Головка молекулы мыла является полярной, что позволяет ей притягиваться к воде, а хвостовик – неполярный, что делает его нерастворимым в воде. Такая особенность структуры поверхностно-активных веществ позволяет им образовывать водные растворы, называемые мицеллами.
Когда мыло наносится на поверхность, молекулы мыла организуются в мицеллы, которые оптимально распределяются по поверхности. Вода притягивается к головкам молекул мыла, тогда как грязь и масло попадают внутрь мицеллы, благодаря нерастворимости хвостовиков в воде. Таким образом, мыло эффективно отделяет грязь от поверхности и образует эмульсию, которая легко смывается водой.
Структура мыла

Основными компонентами мыла являются жиры и масла, которые могут быть растительного или животного происхождения. Жиры содержат молекулы, называемые жирными кислотами, которые имеют гидрофобную (водоотталкивающую) структуру. Это означает, что они не растворяются в воде.
Однако, чтобы мыло могло раствориться, в его структуре присутствуют еще и гидрофильные (водорастворимые) группы. Такие группы могут вступать во взаимодействие с водой и помогать растворить жирные кислоты.
Структура мыла состоит из молекул, называемых мицеллами. Мицеллы представляют собой структуру, в которой гидрофильные группы обращены в сторону воды, а гидрофобные группы свернуты и обращены друг к другу. Такая архитектура позволяет мылу эффективно смывать грязь и масло с поверхности.
Когда мыло наносится на поверхность, мицеллы охватывают грязь и масло, а затем с помощью воды эта смесь смывается с поверхности. Гидрофильные группы мицелл помогают растворить грязь и масло, а гидрофобные группы позволяют им оставаться свернутыми и не растворяться в воде.
Таким образом, структура мыла обеспечивает его эффективность при очищении поверхностей. Молекулы мыла взаимодействуют с грязью и маслом, образуя структуры мицелл, которые смываются с поверхности вместе с водой.
Гидрофильность и гидрофобность
Гидрофильность - это свойство вещества притягивать воду и легко растворяться в ней. В то же время, гидрофобность обозначает отталкивание воды и невозможность растворения в ней.
Итак, почему мыло так эффективно моет поверхности? Ответ кроется в его структуре и химическом составе. Мыло состоит из молекул, которые обладают двумя различными частями: гидрофильной и гидрофобной.
Гидрофильная часть молекулы мыла притягивает воду и образует с ней водородные связи. Это позволяет мылу растворяться в воде и создавать равномерное распределение по поверхности. Частички грязи и жира, захваченные в этом процессе, также притягиваются гидрофильной частью мыла и остаются «заключенными» в водяной среде.
Гидрофобная часть молекулы, напротив, не смешивается с водой и отталкивает ее. Она направлена наружу и позволяет мылу образовывать пленку на поверхности, которая не пропускает воду. Это позволяет мылу легко смывать грязь и жир, так как они приклеены к гидрофобным частицам и могут быть легко смыты водой.
Кроме того, мыло обладает еще одним важным свойством - поверхностной активностью. Это означает, что оно может снижать поверхностное натяжение воды, облегчая процесс смачивания и распределения по поверхности. Таким образом, мыло ускоряет перемещение грязи и жира с поверхности и облегчает их удаление.
В результате, благодаря сочетанию свойств гидрофильности, гидрофобности и поверхностной активности, мыло становится эффективным моющим средством, которое может эффективно очищать различные поверхности от загрязнений.
| Гидрофильность | Гидрофобность |
|---|---|
| Притягивает воду и растворяется в ней | Отталкивает воду и не растворяется в ней |
| Создает равномерное распределение мыла на поверхности | Формирует пленку, не пропускающую воду |
| Притягивает грязь и жир к мылу | Приклеивает грязь и жир к себе |
| Смачивает и облегчает распределение по поверхности | Облегчает смывание грязи и жира |
Действие молекул мыла
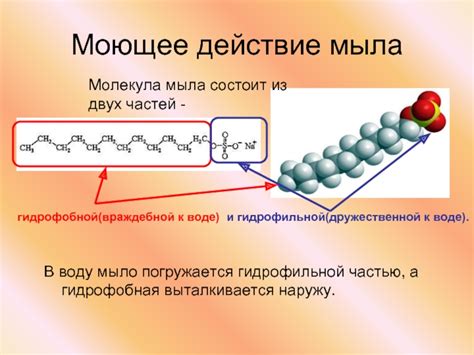
Действие мыла в процессе умывания или мойки основано на уникальных свойствах его молекул. Молекулы мыла состоят из двух частей: гидрофильной и гидрофобной.
- Гидрофильная часть молекулы мыла притягивается к воде и легко смачивается. Эта часть обеспечивает мылу возможность смешаться с водой и образовать равномерный раствор.
- Гидрофобная часть молекулы мыла, напротив, отталкивается от воды и притягивается к грязи, маслу и другим загрязнениям, которые не растворяются в воде. Гидрофобные части молекул мыла образуют микроскопические структуры, называемые мицеллами.
Когда мыло наносится на поверхность, гидрофобные мицеллы образуют покрытие вокруг масляных загрязнений или грязи. Такое покрытие позволяет масляным частицам оставаться вместе и в то же время обеспечивает их удаление с поверхности.
Когда мы втираем мыло в поверхность и массируем ее, молекулы мыла создают между собой электрические заряды, что дополнительно способствует очищению поверхности. Мицеллы мыла также разрушают поверхностное натяжение воды, что позволяет воде лучше проникать в загрязнения и удалять их.
Таким образом, действие молекул мыла заключается в том, что гидрофильная часть притягивает воду, а гидрофобная часть притягивает загрязнения, что способствует эффективному очищению поверхностей от масляных осадков и грязи.
Межкаплярное натяжение
Поверхность жидкости представляет собой слой молекул, которые притягиваются друг к другу силами взаимодействия. Эти силы создают своего рода "покров" на поверхности жидкости, который делает ее тяжело проницаемой для других веществ. Однако, когда в жидкость добавляются ПАВы, они проникают в покров молекул на поверхности и разрушают его.
Молекулы ПАВов имеют особую структуру, которая состоит из двух частей: полюсной и неполярной. Полюсная часть молекулы притягивается к воде, а неполярная - к маслу и другим грязевым частицам. Эта двойственность структуры ПАВов является ключевым фактором, который делает мыло эффективным в очищении поверхностей.
Когда мы моем поверхность с мылом, молекулы ПАВов образуют слой на поверхности грязи или вещества, которое не смешивается с водой. Пяропулярная часть молекул привлекает молекулы воды, что позволяет легко смыть грязь. Неполярная часть молекул его притягивает, что помогает разрушить покров грязи и сделать ее растворимой в воде. Таким образом, мыло осуществляет эффективное моющее действие, благодаря своей способности устранять межкаплярное натяжение и смывать грязь с поверхности.
Смачивание и проникание
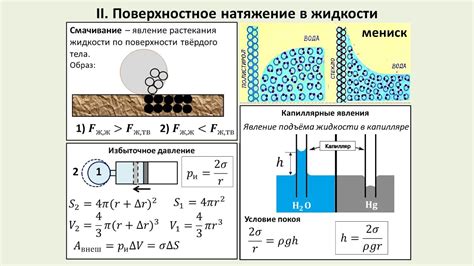
Микроскопические пузырьки, образовавшиеся от мыла, имеют специальное строение. Они состоят из гидрофильной головки (любящая воду) и гидрофобного хвоста (не любящий воду). Гидрофильные головки притягивают воду, тогда как гидрофобные хвосты отталкивают ее.
При нанесении мыла на поверхность, гидрофильные головки взаимодействуют с водой, позволяя пузырькам удерживать влагу. В то время как пузырьки переносятся по поверхности, их гидрофобные хвосты проникают в загрязнения и микробы. Это возможно благодаря тому, что гидрофобные хвосты отталкиваются от воды и предпочитают проникнуть в другие гидрофобные вещества, такие как жир и масло, которые находятся на поверхности.
Сочетание смачивания и проникания позволяет мылу эффективно удалять загрязнения и микробы с поверхностей. При механическом трении, например, при натирании рук или использовании губки, пузырьки мыла с легкостью слетают с поверхности, вместе с собой унося загрязнения и микробы.
Именно этот механизм делает мыло таким незаменимым средством для чистки и гигиены. Благодаря своим свойствам смачивания и проникания, оно способно эффективно очищать самые разные поверхности и защищать нас от бактерий и вирусов.
Электростатическое взаимодействие
Помимо поверхностного натяжения, межмолекулярные силы электростатического взаимодействия играют важную роль в процессе очищения, когда мы моем поверхности с помощью мыла.
Электростатическое взаимодействие основано на привлекательных и отталкивающих силах между заряженными частицами. Поверхности наших рук и поверхности, с которыми мы взаимодействуем, обычно несут некоторым образом заряды. Вода и мыло, в свою очередь, также могут быть заряжены.
При нанесении мыла на поверхность, заряженные частицы в мыле притягиваются к заряженным частицам на поверхности. Это создает электростатические силы, которые помогают удалить загрязнения и придать поверхности более гладкое состояние. Благодаря электростатическому взаимодействию, мыло способно притягивать и удерживать мелкие частицы загрязнений, что облегчает их удаление из поверхности.
Электростатическое взаимодействие также продолжает действовать даже после смывания мыла с поверхности. Заряженные частицы, оставшиеся на поверхности, могут притягивать другие частицы, что предотвращает появление новых загрязнений на поверхности.
Таким образом, электростатическое взаимодействие играет важную роль в эффективности мыла при очищении поверхностей. Грязь и загрязнения притягиваются и удерживаются заряженными частицами мыла, что облегчает их удаление и поддержание поверхности в чистом состоянии.
Разрушение масел и жиров

Когда мыло вступает в контакт с водой, оно образует мицеллы - сферические структуры из молекул мыла, в которых гидрофобные хвосты молекул мыла направлены внутрь, а гидрофильные головки обращены наружу. Гидрофобные хвосты мыла притягиваются друг к другу, в то время как гидрофильные головки образуют внешнюю оболочку мицеллы.
При нанесении мыла на поверхность, мицеллы обволакивают частицы масла или жира, разрушая их агрегаты и образуя эмульсию. Гидрофильные головки мыла притягиваются к водным молекулам, в то время как гидрофобные хвосты связываются с частичками масла или жира. Это позволяет легко смывать загрязнения с поверхности и удалять их вместе с водой.
| Мыло | Вода | Масло/жир |
| Гидрофильная головка | Молекулы воды | |
| Гидрофобный хвост | Частицы масла/жира | |
| Мицелла | Эмульсия |
Кроме того, мыло также содержит вещества, называемые поверхностно-активными веществами или ПАВ. Эти вещества также способны проникать в загрязнения и разрушать их, делая их легкими для удаления с поверхности. ПАВ увеличивают моющие свойства мыла и помогают эффективно очищать различные поверхности.
В результате взаимодействия молекул мыла с водой и загрязнениями, мыло эффективно разрушает масла и жиры, образуя эмульсию, которая легко смывается с поверхности. Использование мыла позволяет удалять даже самые стойкие загрязнения и поддерживать поверхности чистыми и сияющими.
Удаление загрязняющих частиц
Когда мы массируем мылом поверхность, молекулы мыла образуют микроскопические пузырьки, которые проникают в загрязнение и поднимают его над поверхностью. Эти пузырьки включают в себя гидрофобные и гидрофильные части, которые помогают связать загрязняющие частицы с водой и смывать их с поверхности.
Другим важным аспектом является то, что мыло обладает поверхностно-активными веществами, такими как содиум-лаурет-сульфат или кокоил-изетионат. Эти вещества позволяют мылу создавать мицеллы - структуры, которые обволакивают загрязнение и позволяют ему быть растворимым в воде. Когда мы смываем мыло с поверхности, мицеллы с загрязнением удаляются вместе с водой, обеспечивая глубокую очистку.
Кроме того, мыло обладает противомикробными свойствами, которые помогают уничтожить бактерии и вирусы на поверхности. Способность мыла удалять загрязнения и микроорганизмы делает его идеальным средством для поддержания гигиены и чистоты поверхностей, особенно в условиях повышенной заразности.
| Преимущества удаления загрязняющих частиц с помощью мыла: |
|---|
| • Глубокая очистка поверхностей |
| • Удаление бактерий и вирусов |
| • Безопасно для использования на различных поверхностях |
| • Доступность и низкая стоимость |
Биоразлагаемость и безопасность

Мыло, которое не является биоразлагаемым, может содержать химические соединения, токсичные для живых организмов. Такие вещества могут наносить вред окружающей среде и оказывать отрицательное влияние на здоровье человека.
Помимо биоразлагаемости, безопасность также является важным аспектом при выборе мыла. Качественное мыло должно быть нежным к коже и не вызывать раздражения или аллергических реакций.
Пользуясь биоразлагаемым и безопасным мылом, мы не только чистим и защищаем нашу кожу, но и заботимся о природе и своем здоровье.




