Хлорид водорода (HCl) - это одна из популярных неорганических химических соединений, которая нашла широкое применение в различных отраслях науки и промышленности. Возникает вопрос: как классифицировать эту химическую суbстанцию - как оксид, основание, кислота или соль? Чтобы разобраться в этом, необходимо изучить основные свойства и реакции HCl.
Стоит отметить, что оксиды являются химическими соединениями, в которых кислород связан с другим элементом. Однако, HCl не содержит кислород и, следовательно, не может быть классифицировано как оксид.
При рассмотрении оснований, важно отметить, что они обычно содержат гидроксильную группу (OH). В HCl нет этой группы, поэтому оксид нельзя отнести к основанию.
Теперь рассматриваем кислоты. Кислота - это вещество, которое в растворе образует ион водорода (H+). В случае с HCl, оно образует водород и хлоридные ионы. Таким образом, HCl можно классифицировать как кислоту.
И, наконец, соли. Соль - это химическое соединение, состоящее из катиона и аниона. HCl - это чистый хлоридный ион (Cl-), поэтому оно не является солью.
Итак, HCl является кислотой, которая находит применение во многих областях, например, в производстве пластмасс, сборке электроники и косметической промышленности.
HCl - вещество, имеющее особые свойства

Соляная кислота имеет сильно выраженные кислотные свойства и широко используется в промышленности, медицине и лабораторных исследованиях. Это химическое соединение обладает высокой коррозионной активностью и используется для очистки металлов и различных поверхностей.
Хлороводород также широко используется для производства солей, таких как хлорид натрия (NaCl) и хлорид кальция (CaCl2). Эти соли применяются в пищевой и промышленности, а также в сельском хозяйстве.
| Наименование | Формула |
|---|---|
| Хлороводород (соляная кислота) | HCl |
| Хлорид натрия (поваренная соль) | NaCl |
| Хлорид кальция | CaCl2 |
Таким образом, HCl является важным веществом, обладающим особенными свойствами и находящим широкое применение в различных отраслях промышленности и научных исследований.
Структура и химические свойства HCl
HCl (хлороводород) представляет собой бинарное соединение из хлора (Cl) и водорода (H). Его молекулярная формула HCl указывает на то, что в одной молекуле присутствуют один атом водорода и один атом хлора.
Молекула HCl является линейной и имеет полярные связи. Водородный атом обладает частично положительным зарядом (+), а хлоровый атом - частично отрицательным зарядом (-). Такая полярность молекулы HCl обуславливает ее особые физические и химические свойства.
HCl - одноатомная кислота, которая может реагировать с основаниями или веществами, обладающими основными свойствами. При таких реакциях происходит образование солей.
Вода является одним из веществ, которое может реагировать с HCl. При их реакции образуется соль - хлорид водорода (HCl) и образуются ионные связи между атомами водорода и кислорода.
| Свойство | Значение |
|---|---|
| Формула | HCl |
| Молярная масса | 36,461 г/моль |
| Температура плавления | -114.22 °C |
| Температура кипения | -85.05 °C |
| Плотность | 1,49 г/см³ |
| Растворимость в воде | разнорастворим в воде |
Физические свойства HCl

Одна из характеристик HCl - его растворимость в воде. Газ легко растворяется в воде, образуя соляную кислоту. Раствор HCl проявляет кислотные свойства: он имеет кислую реакцию, может изменять цвет индикаторов и реагировать с основаниями.
HCl также обладает высокой плотностью. Плотность газового HCl составляет около 1,49 г/л при 0 °C и нормальном атмосферном давлении.
Кроме того, вещество является полярным и образует кристаллическую решетку при низких температурах. HCl также обладает высокими температурными свойствами, имея кипение при -85,1 °C и плавление при -114,2 °C.
Однако следует быть осторожным при работе с HCl, так как это очень токсичное и едкое вещество. Необходимо соблюдать меры предосторожности и использовать защитное снаряжение при работе с ним.
| Свойство | Значение |
|---|---|
| Физическая форма | Газ |
| Цвет | Бесцветный |
| Запах | Резкий, едкий |
| Плотность (при 0 °C и нормальном атмосферном давлении) | 1,49 г/л |
| Температура кипения | -85,1 °C |
| Температура плавления | -114,2 °C |
Применение HCl в промышленности
Одним из основных применений HCl является его использование для производства хлорида натрия (NaCl), который широко используется в пищевой промышленности, химической промышленности и других отраслях.
Одной из крупных отраслей, где применяется HCl, является нефтеперерабатывающая промышленность. Хлороводородная кислота используется для обработки нефти и газа, а также для очистки и обезвреживания различных отходов и сточных вод.
HCl также применяется в производстве промышленных химикатов, таких как хлор и хлорныепроизводные. Хлор является важным сырьем для производства пластиков, резин, хлорорганических соединений и многих других продуктов.
Другим важным применением HCl является его использование в гальванической промышленности для очистки и обработки металлических поверхностей, а также для регенерации обезвреживающих растворов.
HCl также применяется в текстильной промышленности для обработки и окрашивания тканей, а также для регенерации различных химических растворов.
В общем, HCl является важным реагентом в промышленности и находит широкое применение в различных отраслях, включая нефтепереработку, производство химикатов, гальваническую и текстильную промышленности.
| Отрасль | Применение HCl |
|---|---|
| Нефтеперерабатывающая промышленность | Обработка нефти и газа, очистка сточных вод |
| Химическая промышленность | Производство хлорида натрия и других химических соединений |
| Гальваническая промышленность | Обработка металлических поверхностей |
| Текстильная промышленность | Обработка тканей и окрашивание |
HCl - оксид или неоксид?
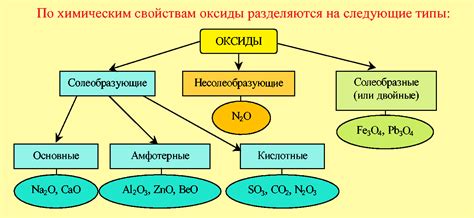
Однако HCl (хлороводородная кислота) не является оксидом, так как HCl не содержит кислорода. HCl - это кислота, состоящая из водорода и хлора.
Хлороводородная кислота является сильной кислотой и образуется при растворении водорода в воде. Она широко используется в промышленности и лабораториях, а также в медицине.
Химическая формула HCl
Хлороводород является кислотой, образуя раствор с кислотными свойствами. При диссоциации в водном растворе, HCl образует ион водорода (H+) и ион хлорида (Cl-), делая его кислотой.
HCl также может быть использован как основание, принимая водород и образуя ион гидрида (H-) в присутствии сильных оснований.




