Органическая химия изучает разнообразие соединений, состоящих из углерода и других элементов. Два распространенных класса органических соединений - гомологи и изомеры - обладают сходством в составе элементов, но отличаются в строении и свойствах. Понимание различий между гомологами и изомерами является ключевым для понимания структуры и функции органических соединений.
Гомологи - это серия соединений, в которых каждый последующий член отличается от предыдущего на константную единицу, такую как -CH2-. Например, серия простых насыщенных углеводородов: метан (CH4), этан (C2H6), пропан (C3H8) и так далее. Гомологи имеют сходные химические свойства и демонстрируют градиентные изменения в физических свойствах, таких как температура кипения и плотность, по мере увеличения размера молекулы.
Изомеры, с другой стороны, являются соединениями, содержащими одинаковое количество атомов и те же элементы, но обнаруживают различное строение молекул. Изомеры различаются как в пространственной конфигурации, так и в расположении атомов. Например, изомеры бутана могут быть представлены двумя формами - нормальным бутаном и изобутаном. Они имеют одинаковую молекулярную формулу C4H10, но расположение углеродных скелетов различно, что ведет к их различным свойствам и реакционной активности.
Гомологи и изомеры: определение и различия
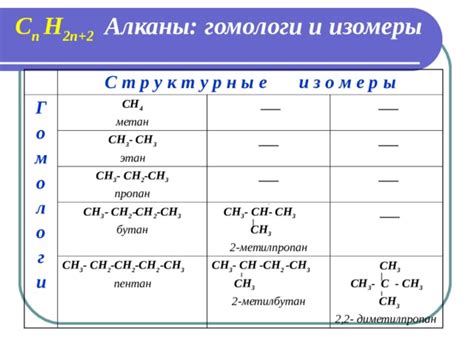
Гомологи представляют собой ряд соединений, которые имеют одинаковую функциональную группу и изменяются только по размеру углеводородной цепи. Например, серия алканов - метан, этан, пропан и т.д. В этом случае, каждое следующее соединение отличается от предыдущего на один метиловый (CH2) остаток.
Изомеры, с другой стороны, представляют собой различные соединения с одним и тем же атомным составом, но разными атомными или молекулярными структурами. Например, изомерия может проявляться в различной расположении атомов в молекуле, вращении молекулы вокруг связей или наличии разных функциональных групп.
Основное отличие между гомологами и изомерами заключается в изменении угловой группы и размере углеводородной цепи в гомологах, в то время как в изомерах изменяется внутренняя структура молекулы. Эти различия внутренней структуры и функциональных групп могут привести к изменению свойств и реакционной способности молекул.
Например, гомологи алканов обладают сходными химическими свойствами, так как имеют одну и ту же функциональную группу - метильную группу (CH3). Однако, их физические свойства, такие как температура кипения и границы смачиваемости, изменяются с увеличением размера углеводородной цепи.
С другой стороны, изомеры имеют разные свойства и взаимодействия. Например, изомеры бутана - нормальный бутан и изобутан - имеют разные точки кипения и свойства сжигания, так как их атомы углерода расположены в разном порядке.
В целом, гомологи и изомеры представляют различные типы органических соединений, которые отличаются по своей структуре и свойствам. Понимание этих различий помогает в изучении и понимании органической химии и ее роли в живых системах.
Гомологи: определение и примеры
Примером гомологов является серия органических соединений альканов - метан (CH4), этан (C2H6), пропан (C3H8), бутан (C4H10) и так далее. Все они имеют одну и ту же общую формулу CnH2n+2 и отличаются только числом атомов углерода в молекуле.
Еще одним примером гомологов являются серия альдегидов - метаналь (HCHO), этаналь (CH3CHO), пропаналь (CH3CH2CHO) и так далее. Все они имеют атомарную структуру, включающую альдегидную группу (-CHO), но отличаются по длине углеродной цепи.
Таким образом, гомологи представляют собой серию химических соединений с общей атомной структурой, но отличающихся по своей формуле и смещении структурных элементов.
Изомеры: определение и примеры
Примером изомерии является бутан и изобутан. Оба соединения имеют молекулярную формулу C4H10, но их структуры различаются. Бутан имеет прямую цепь углеродных атомов, тогда как изобутан имеет разветвленную цепь. Эти изомеры обладают разными физическими свойствами и реакционной активностью.
Другим примером изомерии является глюкоза и фруктоза. Оба соединения имеют молекулярную формулу C6H12O6, но их структуры и свойства различаются. Глюкоза является альдозой, тогда как фруктоза - кетоза. Эти изомеры являются сложными сахарами и играют важную роль в биохимических процессах организма.
Изомеры имеют большое значение в органической химии, так как даже небольшие изменения в структуре могут привести к различным свойствам и реакционной активности соединений.




