Химия - это наука, изучающая строение, состав и свойства вещества, а также изменение, которые они могут претерпевать. В химии существуют различные группы элементов, которые имеют свои особенности и свойства. Одной из таких групп является металлы главной подгруппы 2 группы.
Металлы главной подгруппы 2 группы представлены такими элементами, как магний (Mg), цинк (Zn), кальций (Ca). Они обладают рядом общих свойств, которые делают их ценными и широкоиспользуемыми в различных областях нашей жизни. Например, они являются хорошими проводниками электричества и тепла, образуют прочные сплавы и легко соединяются с другими элементами.
Чтобы углубить свои знания по химии и проверить свою эрудицию, предлагаем вам пройти тест по металлам главной подгруппы 2 группы. Вам будет предложено несколько вопросов, в которых вам нужно будет выбрать правильный ответ. Удачи!
Основные свойства металлов

Проводимость
Одним из основных свойств металлов является их высокая электропроводность. Они легко передают электрический ток по своей структуре, так как атомы в металлах формируют гидриды металлов.
Пластичность и формоизменяемость
Металлы обладают свойством пластичности, то есть способностью легко изменять форму под действием внешних сил, без разрушения своей структуры. Благодаря этому, металлы могут быть легко обработаны и использованы для создания различных изделий.
Тепло- и электропроводность
Металлы также обладают высокой теплопроводностью. Они могут легко передавать тепловую энергию по своей структуре. Это делает их хорошими материалами для создания теплопроводящих устройств, таких как радиаторы или провода. Кроме того, металлы обладают высокой электропроводностью, благодаря которой они часто используются в электрических проводах и контактах.
Магнитные свойства
Некоторые металлы являются магнитными и обладают способностью притягиваться к магниту или обладают свойством самомагнитения. Это свойство делает их полезными в применении для создания магнитов, электромагнитов и других устройств, которые используют магнитные поля.
Высокая плотность и твердость
Металлы обладают высокой плотностью, что означает, что они имеют большую массу по сравнению с объемом. Однако, несмотря на высокую плотность, многие металлы также обладают высокой твердостью – способностью сопротивляться деформации и истиранию. Это делает их прочными и долговечными материалами для различных конструкций и инженерных решений.
| Металлы | Проводимость | Пластичность и формоизменяемость | Тепло- и электропроводность | Магнитные свойства | Плотность и твердость |
|---|---|---|---|---|---|
| Железо | Да | Да | Да | Нет | Высокая |
| Алюминий | Да | Да | Да | Нет | Средняя |
| Медь | Да | Да | Да | Нет | Средняя |
Физические и химические свойства
Металлы главной подгруппы 2 группы – это элементы, обладающие рядом характерных физических и химических свойств.
Физические свойства металлов главной подгруппы 2 группы определяются их металлическим строением и атомными структурами. Эти металлы обладают высокой пластичностью и термической и электрической проводимостью. Они обладают блестящей поверхностью, способностью отталкивать магнитный поток и хорошей теплопроводностью. Они также обладают высокой плотностью и температурой плавления.
Химические свойства металлов главной подгруппы 2 группы характеризуются их восприимчивостью к химическим реакциям. Эти металлы легко реагируют с кислородом, образуя оксиды. Они также активно взаимодействуют с кислотами, образуя соли. Некоторые металлы восстанавливаются с водородом, а некоторые - с водой. Металлы подвержены коррозии под влиянием агрессивных сред, что делает их устойчивыми к разрушению.
Таким образом, металлы главной подгруппы 2 группы проявляют ряд характерных физических и химических свойств, которые делают их уникальными материалами с широким спектром применения в различных сферах жизни.
Примеры металлов главной подгруппы 2 группы
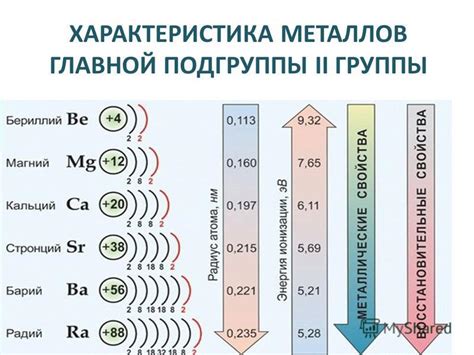
Металлы главной подгруппы 2 группы таблицы д.и.с. (добавок к классификации химических элементов, разработанной в 1994 году Международным союзом по чистой и прикладной химии) включают в себя металлы-алкалоземельцы, которые имеют 2 валентных электрона на внешней энергетической оболочке. Примеры таких металлов: магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra).
Магний (Mg) – серебристо-белый металл, который является очень легким и сравнительно мягким. Он обладает высокой пластичностью и хорошей проводимостью электричества. Один из наиболее распространенных элементов в земной коре, магний широко используется в промышленности для производства сплавов, сталей, алюминия и многих других материалов.
Кальций (Ca) – блестящий серебристо-белый металл, который является важным элементом для многих живых организмов. Он составляет значительную часть нашего организма, входит в состав костей, зубов и играет важную роль в многих биологических процессах. Кальций также широко применяется как добавка в пищу, в качестве строительного материала и в других отраслях промышленности.
Стронций (Sr) – серебристо-белый металл, который обладает схожими свойствами с кальцием. Он используется в производстве пиротехники, стекла, ядерных реакторов и других технологических процессах. Стронций также является радиоактивным элементом и используется в медицине для лечения рака.
Барий (Ba) – серебристо-белый металл, который имеет высокую плотность и тугоплавкость. Он используется в производстве сплавов, стала, электрических проводов и других материалов. Барий также использовался в прошлом в медицине для рентгеновских исследований. В настоящее время его использование ограничено из-за его высокой токсичности.
Радий (Ra) – радиоактивный элемент, который обладает высокой плотностью и является очень тяжелым. Его радиоактивные свойства делают его опасным для здоровья, и поэтому его использование ограничено. Радий был использован в прошлом в радиотерапии для лечения рака, однако сейчас этот метод заменен более безопасными способами лечения.
Свойства металлов главной подгруппы 2 группы
Металлы главной подгруппы 2 группы характеризуются рядом свойств, которые делают их важными и широко применяемыми в различных отраслях промышленности. Вот некоторые из этих свойств:
- Высокая пластичность: металлы главной подгруппы 2 группы обладают способностью изменять свою форму без разрушения. Благодаря этому свойству они широко используются в процессе литья, ковки и проката.
- Химическая активность: эти металлы среднеактивны, что означает их способность реагировать с различными субстанциями. Из-за этого свойства они могут быть использованы как катализаторы в различных химических реакциях.
- Высокая теплопроводность и электропроводность: металлы главной подгруппы 2 группы являются отличными проводниками тепла и электричества. Благодаря этим свойствам они используются в создании теплопроводящих элементов и электрических проводов.
- Низкая температура плавления: многие металлы главной подгруппы 2 группы имеют низкую температуру плавления, что облегчает их обработку и использование в различных технологических процессах.
- Устойчивость к коррозии: некоторые металлы этой группы обладают высокой устойчивостью к окислению и коррозии. Это делает их незаменимыми материалами для создания различных конструкций и изделий, которые подвержены воздействию влаги и агрессивных сред.
Разумное использование этих свойств металлов главной подгруппы 2 группы позволяет использовать их в различных отраслях промышленности, а также в бытовых и научных целях.
Кислотные свойства металлов главной подгруппы 2 группы
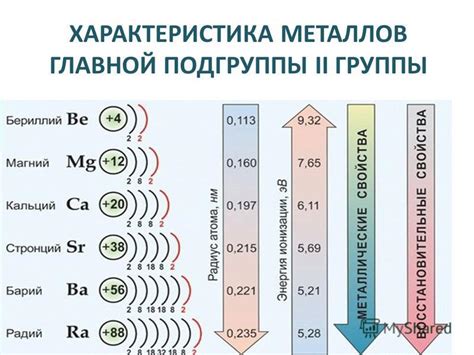
Металлы главной подгруппы 2 группы характеризуются высокой активностью и способностью образовывать соединения с кислородом.
Эти металлы, такие как магний, цинк, кадмий и марганец, реагируют с кислородом из воздуха, образуя оксиды. Например, магний горит на воздухе, образуя белую пыль магния оксида (MgO).
Металлы главной подгруппы 2 группы также реагируют с кислотами, образуя соли и выделяя водород. Например, цинк реагирует с соляной кислотой, образуя хлорид цинка и выделяя водородный газ:
Zn + 2 HCl → ZnCl2 + H2
Кроме того, металлы главной подгруппы 2 группы могут растворяться в растворах щелочей, образуя гидроксиды. Например, марганец реагирует с раствором натрия гидроксида, образуя гидроксид марганца (II) и выделяя водородный газ:
2 Mn + 6 NaOH → 2 Na3MnO4 + 3 H2O
- Металлы главной подгруппы 2 группы проявляют кислотные свойства в реакции с кислотами.
- Они образуют оксиды при взаимодействии с кислородом.
- Металлы данной группы могут растворяться в растворах щелочей, образуя гидроксиды.
Получение металлов главной подгруппы 2 группы
Металлы главной подгруппы 2 группы – это химический элементы, которые находятся во второй подгруппе периодической системы. Здесь включены металлы, такие как магний, кальций, стронций, барий и радий.
Магний получают из минералов, содержащих его в виде оксидов и сульфидов. Смешанные оксиды магния с железом, называемые серпентином, являются одним из наиболее распространенных источников магния. Кроме того, магний можно получить путем электролитического восстановления его солей, таких как хлорид и сульфат.
Кальций получают из его оксида или карбида путем восстановления алюминием или другими металлами. Иногда кальций можно извлечь также из природного минерала гипса.
Стронций и барий получают похожими методами на получение кальция. Их оксиды или карбиды восстанавливают другими металлами или алюминием.
Радий – это редкоземельный элемент и самый тяжелый из металлов главной подгруппы 2 группы. Получение радия является сложным процессом, включающим различные химические реакции и охлаждение.
Вопрос-ответ
Какие элементы относятся к металлам главной подгруппы 2 группы?
К металлам главной подгруппы 2 группы относятся бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra).
Каковы основные свойства металлов главной подгруппы 2 группы?
Основные свойства металлов главной подгруппы 2 группы: они обладают серебристо-белым цветом, хорошей теплопроводностью и электропроводностью, образуют двухатомные ионные катионы, обладают низкой активностью.
Какие соединения образуют металлы главной подгруппы 2 группы?
Металлы главной подгруппы 2 группы образуют соединения с различными элементами. Например, они образуют оксиды (BeO, MgO), гидроксиды (Mg(OH)2, Ca(OH)2), сложные оксиды (Ca3(PO4)2, Sr(NO3)2), сульфаты (BaSO4) и другие.
Каким образом используются металлы главной подгруппы 2 группы?
Металлы главной подгруппы 2 группы имеют широкое применение в различных отраслях промышленности. Например, магний используется в производстве автомобилей, космической и аэрокосмической отраслях; кальций применяется в производстве стекла и строительных материалов; барий используется в производстве радиолюминесцентных красителей для телевизоров и компьютерных мониторов.
Какие особенности у металлов главной подгруппы 2 группы?
Металлы главной подгруппы 2 группы имеют ряд особенностей. Например, они обладают высокой пластичностью и ковкостью, что делает их легко обрабатываемыми; они образуют стабильные ионы с положительными зарядами; они имеют высокую плотность и температуру плавления. Кроме того, магний и его сплавы имеют низкую плотность и применяются в производстве легких конструкций, например, в авиации и автомобилестроении.
