Соляная кислота, или хлоридная кислота, является одной из наиболее распространенных и важных неорганических кислот. Она обладает сильной кислотной реакцией и широко используется в промышленности, лабораториях и быту. Одним из особенностей этой кислоты является ее взаимодействие с металлами, которое обусловлено ее химическими свойствами и механизмом реакции.
Взаимодействие соляной кислоты с металлами осуществляется путем их растворения. Кислота реагирует с поверхностью металла, образуя соли и выделяя водород. Этот процесс называется коррозией металла и является одной из основных причин разрушения различных конструкций и оборудования.
Однако, не все металлы взаимодействуют с соляной кислотой одинаково. Некоторые металлы, такие как серебро, цинк и натрий, не растворяются в соляной кислоте или реагируют очень медленно. Это связано с тем, что эти металлы обладают защитной оксидной пленкой на своей поверхности, которая предотвращает их взаимодействие с кислотой. Поэтому, соляная кислота может использоваться для очистки металлов от загрязнений без их дальнейшего разрушения.
Металлы и химические реакции
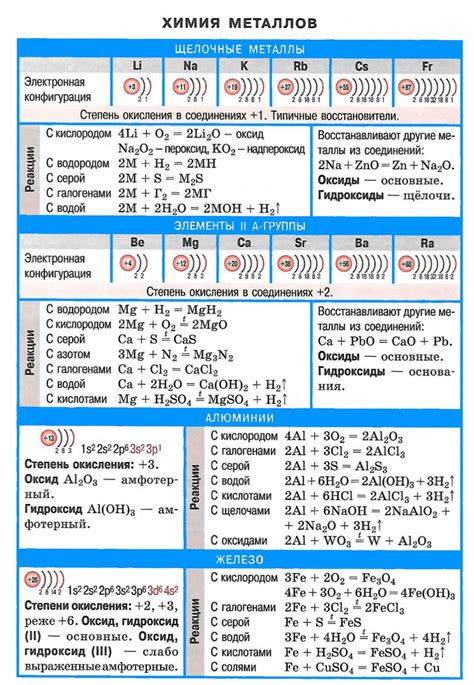
Металлы являются важным классом химических элементов, которые обладают хорошей электропроводностью и химической реакционной способностью. Благодаря этим свойствам, они могут вступать во взаимодействие с различными веществами, включая кислоты.
Одной из наиболее распространенных химических реакций, в которых участвуют металлы, является их взаимодействие с кислотами. Как правило, металлы реагируют с кислотами, образуя соли и выделяя водородный газ.
С одной стороны, металлы имеют тенденцию отдавать электроны, образуя положительно заряженные ионы (катионы). Это позволяет им вступать во взаимодействие с отрицательно заряженными ионами анионами) кислоты.
С другой стороны, у кислот есть тенденция принимать электроны, образуя отрицательно заряженные ионы (анионы). Это позволяет им вступать во взаимодействие с положительно заряженными ионами (катионами) металлов.
Однако, не все металлы вступают во взаимодействие с кислотами одинаково. Некоторые металлы, такие как серебро, цинк и натрий, обладают низкой реакционной способностью с кислотами. Это связано с их химическими свойствами и электрохимическим потенциалом.
Соляная кислота: основные свойства и применение
Соляная кислота – это химическое соединение с формулой HCl, известное также как хлороводородная кислота. Она является одной из наиболее распространенных и важных кислот, используемых в химической промышленности.
Основные свойства соляной кислоты заключаются в ее летучести, высокой растворимости в воде и сильной кислотности. Кислотные свойства HCl обусловлены ее способностью отдавать водородные ионы (H+) при растворении. Это делает соляную кислоту важным реагентом во многих химических процессах и лабораторных исследованиях.
Соляная кислота имеет широкое применение в промышленности, медицине и лабораторной практике. Она широко используется в процессах очистки металлов, производстве пластмасс, текстильной и нефтеперерабатывающей промышленности.
Соляная кислота также используется для регулирования pH водных растворов, а также в качестве компонента при производстве удобрений, фотопленок и кожных средств.
При работе с соляной кислотой необходимо соблюдать особую осторожность, так как она относится к категории опасных веществ. При попадании на кожу или в глаза она может вызвать ожоги. Также необходимо избегать контакта с другими химическими веществами, так как это может привести к опасным реакциям.
Химическое взаимодействие соляной кислоты с металлами
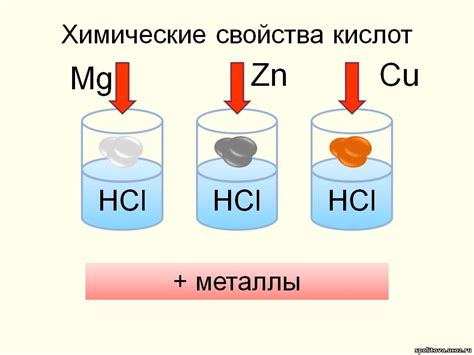
Соляная кислота, или хлороводородная кислота (HCl), представляет собой одну из наиболее распространенных и сильных минеральных кислот. Ее химическое взаимодействие с металлами может протекать различными способами в зависимости от свойств металла и условий реакции.
При взаимодействии соляной кислоты с рядом металлов, например, железом, алюминием или цинком, происходит образование солей и выделение водорода. Эти реакции протекают с выделением тепла и сопровождаются плавлением металла.
Однако соляная кислота не взаимодействует с некоторыми металлами, такими как серебро, цинк и натрий. Это объясняется тем, что эти металлы обладают достаточно низкой реакционной способностью и не способны вытеснить водород из кислоты. Соляная кислота не оказывает коррозионного воздействия на поверхность этих металлов.
Таблица Кислотно-основные свойства металлов позволяет оценить возможность и характер реакции хлороводородной кислоты с различными металлами. Некоторые металлы проявляются активно при взаимодействии с соляной кислотой, образуя соли и выделяя водород, в то время как другие металлы амфотерны и образуют соли, но без выделения водорода. Некоторые металлы, такие как серебро, цинк и натрий, не реагируют с соляной кислотой вообще.
Взаимодействие с серебром: особенности
Соляная кислота обладает высоким кислотным свойством, поэтому взаимодействие ее с серебром характеризуется особыми особенностями. При контакте с металлическим серебром происходит образование соляного соединения - хлорида серебра (AgCl).
Хлорид серебра обладает низкой растворимостью в воде, поэтому при взаимодействии с соляной кислотой образуется прочный осадок, который трудно растворяется. Это свойство использовалось в прошлом для выделения и очистки серебра из руды и сплавов.
Однако, важно учесть, что образование осадка хлорида серебра при взаимодействии соляной кислоты со серебром происходит только в присутствии хлорных ионов. Так как обычно соляная кислота не содержит хлоридных примесей, для успешного взаимодействия необходимо добавлять дополнительный источник хлорных ионов, например, хлорид натрия.
Таким образом, взаимодействие серебра с соляной кислотой требует наличия дополнительных хлоридных ионов, а образующийся осадок хлорида серебра является хорошим показателем наличия серебра в исследуемой смеси или растворе.
Взаимодействие с цинком: особенности

Соляная кислота активно взаимодействует с металлами, и цинк не является исключением. В процессе взаимодействия соляной кислоты и цинка происходит образование соли цинка (хлорида цинка) и освобождение водорода. Реакция протекает по следующему уравнению: 2HCl + Zn -> ZnCl2 + H2
Одной из особенностей взаимодействия соляной кислоты и цинка является обратимость реакции. При наличии достаточного количества соляной кислоты, происходит полное растворение цинка, что позволяет получать хлорид цинка с высокой степенью очистки. При уменьшении концентрации кислоты или ее отсутствии, реакция может идти в обратную сторону: хлорид цинка реагирует с водой, образуя цинк гидроксид и соляную кислоту.
Взаимодействие соляной кислоты и цинка можно использовать для получения водорода. Образующийся водород является горючим газом и может быть использован в различных промышленных и химических процессах. Взаимодействие соляной кислоты и цинка можно проводить как в аппарате с непрерывной подачей реагентов, так и в пакетном режиме, в зависимости от требуемого объема и скорости процесса.
При взаимодействии соляной кислоты и цинка важно учитывать, что реакция протекает с выделением большого количества тепла. Поэтому необходимо соблюдать меры предосторожности при проведении данного эксперимента, такие как использование защитных очков, перчаток и других средств индивидуальной защиты. Также следует обратить внимание на правильную организацию отвода освобождающегося водорода, чтобы избежать опасности возгорания или взрыва.
Взаимодействие с натрием: особенности
Соляная кислота демонстрирует особенности взаимодействия с натрием, которые отличаются от ее реакции с другими металлами, такими как серебро и цинк.
Во-первых, соляная кислота при контакте с натрием происходит очень быстро и интенсивно. Этот процесс сопровождается выделением пузырьков газа, который образуется в результате реакции хлорида натрия и воды. Гидролиз натрия приводит к образованию гидроксида натрия, который реагирует с кислотой и образует хлорид натрия и воду.
Во-вторых, взаимодействие соляной кислоты с натрием обладает характерными свойствами, такими как образование натриевых солей. В результате этого процесса образуется хлорид натрия, который является одной из наиболее распространенных солей натрия. Он обладает высокой растворимостью в воде и широко используется в различных отраслях промышленности и бытовой химии.
Таким образом, взаимодействие соляной кислоты с натрием отличается своей интенсивностью и образованием натриевых солей. Это делает натрий одним из важных компонентов в промышленных процессах и химических реакциях, связанных с использованием соляной кислоты.
Вопрос-ответ
Какие металлы реагируют с соляной кислотой?
С соляной кислотой реагируют такие металлы, как алюминий, железо, свинец, медь, никель и многие другие. Однако, серебро, цинк и натрий являются исключениями, так как они не реагируют с соляной кислотой.
Почему серебро не реагирует с соляной кислотой?
Серебро не реагирует с соляной кислотой из-за своей высокой стабильности и низкой активности. Оно обладает низкой степенью реакционной способности и устойчиво к действию кислоты.
Почему цинк не реагирует с соляной кислотой?
Цинк не реагирует с соляной кислотой из-за образования защитной оксидной пленки на его поверхности. Эта пленка предотвращает дальнейшее взаимодействие цинка с кислотой.
Какую роль играет натрий во взаимодействии с соляной кислотой?
Натрий имеет низкую реакционную способность и не реагирует с соляной кислотой. Однако, он может образовывать с соляной кислотой соль - хлорид натрия. Это реакция нейтрализации.
Какие металлы реагируют с соляной кислотой наиболее интенсивно?
Между металлами и соляной кислотой существует разная степень активности. Наиболее интенсивно реагируют металлы, расположенные в верхней части химической активности, такие как алюминий, железо, цинк, медь. Они способны активно взаимодействовать с кислотой и образовывать соли и водород.
