Реакция магния (Mg) с соляной кислотой (HCl) является одной из наиболее известных и широко изученных реакций в химической науке. Она относится к классу реакций металлов с кислотами и исследуется как в образовательных учебных целях, так и в промышленности.
Особенностью реакции магния с соляной кислотой является выделение водорода (H2) и образование соли магния (MgCl2). При этом происходит выделение большого количества энергии в виде тепла, что делает эту реакцию яркой и заметной. Реакция проходит довольно быстро и сопровождается сильным шипением и падением пламени.
Интересно отметить, что водород, выделяемый при реакции, можно собрать и использовать в дальнейших исследованиях или применениях. Кроме того, реакция магния с соляной кислотой играет важную роль в производстве металлического магния, так как является одним из этапов в его получении из природного сырья.
Реакция магния с соляной кислотой

Реакция магния с соляной кислотой является типичной реакцией образования солей. Магний (Mg) активный металл и соляная кислота (HCl) — сильная кислота, поэтому взаимодействие между ними протекает достаточно интенсивно.
В результате реакции образуется хлорид магния (MgCl2) и выделяется водородный газ (H2). Хлорид магния имеет вид белых кристаллических зерен или порошка и хорошо растворяется в воде.
Проявление реакции можно наблюдать визуально. При взаимодействии магния с соляной кислотой происходит выделение пузырьков газа, а также может наблюдаться изменение цвета раствора с красного на желтый из-за образования оставшегося от реакции хлорида железа.
Важно отметить, что реакция магния с соляной кислотой является экзотермической, то есть сопровождается выделением тепла. Поэтому при проведении этой реакции следует быть осторожным и соблюдать меры безопасности.
Свойства и химический состав магния
Магний (Mg) - химический элемент периодической системы, относящийся к щелочноземельным металлам. В природе его можно найти в виде солей и оксидов, а также в составе многих минералов.
Магний обладает несколькими важными свойствами. Во-первых, он является легким металлом с низкой плотностью - всего 1,74 г/см³. Ёвободном состоянии магний обладает серебристо-белым оттенком и хорошо обрабатывается.
Однако на воздухе магний быстро окисляется и покрывается тонким слоем оксида, который мешает его дальнейшей реакции с кислородом. Магний взаимодействует с водой, но реакция протекает очень медленно, поэтому магний практически не растворим в нейтральной воде.
Химический состав магния также интересен, так как он состоит из одного атома магния. Атомный номер 12 указывает на наличие у него 12 протонов в ядре, а атомный вес равен примерно 24,31 г/моль. Магний также обладает малой электроотрицательностью, что делает его хорошим редуктором во многих химических реакциях.
Магний имеет важное значение в живой природе. Он является необходимым элементом для функционирования многих ферментов и метаболических процессов в организмах живых организмов. Магний содержится в таких продуктах как орехи, зеленые овощи, зерно и морепродукты, и его нехватка может привести к различным заболеваниям.
Описание соляной кислоты и ее реакционных способностей
Соляная кислота (химическая формула HCl) – это одна из самых распространенных и сильнодействующих кислот. Она является бесцветной жидкостью, обладающей острой и едкой пахучестью. Соляная кислота широко используется в различных областях, таких как химическая промышленность, медицина, производство удобрений и пищевая промышленность.
Соляная кислота обладает сильной реакционной способностью, что объясняется ее высокой степенью диссоциации в воде. При контакте с водой соляная кислота расщепляется на ион водорода (H+) и ион хлорида (Cl-). Эта реакция протекает экзотермически, сопровождаясь выделением теплоты.
Основные реакционные способности соляной кислоты связаны с ее способностью образовывать соли, водородные соединения и продукты окисления. При взаимодействии с различными соединениями соляная кислота может вызывать различные химические изменения. Например, она может образовывать хлориды металлов, сульфаты, нитриты и другие соединения.
Реакция магния с соляной кислотой является одной из наиболее известных и широко используемых реакций соляной кислоты. В результате этой реакции образуется хлорид магния (MgCl2) и выделяется водород. Такая реакция протекает очень быстро и с признаками реакции восстановления. При этом магний реагирует с ионами водорода, образуя молекулы воды и освобождая энергию.
Условия и принципы проведения реакции соляной кислоты с магнием
Реакция соляной кислоты с магнием проводится в лаборатории при определенных условиях и соблюдении определенных принципов. Основной способ проведения реакции заключается в помещении порошка магния в реакционную посуду и последующем влевании соляной кислоты.
Перед началом реакции необходимо подготовить реакционную посуду, которая должна быть чистой и сухой. Для этого можно использовать стеклянные или пластиковые колбы или пробирки. В процессе эксперимента важно соблюдать меры безопасности, так как реакция сопровождается выделением газа и высвобождением тепла.
При проведении реакции необходимо держаться определенной последовательности действий. На первом этапе в реакционную посуду помещают порошкообразный магний, который может быть предварительно навеской или разломлен на мелкие кусочки. Затем в медленном темпе вливают в посуду соляную кислоту, при этом образуется пузырьковый газ, который является проявлением реакции.
Реакция соляной кислоты с магнием происходит по следующей химической формуле: Mg + 2HCl = MgCl2 + H2. В результате реакции образуется хлорид магния и молекулы водорода. Выделяющийся газ обладает легким запахом и горючими свойствами, поэтому при проведении реакции следует быть осторожными и работать в хорошо проветриваемом помещении.
Образование и свойства магния хлорида в результате реакции

Магний хлорид (MgCl2) образуется в результате реакции магния с соляной кислотой (HCl). Реакция между данными веществами является типичным примером нейтрализационной реакции.
Магний хлорид представляет собой белый кристаллический порошок, хорошо растворяющийся в воде. Раствор магния хлорида обладает соленоватым вкусом и характерным запахом. Магний хлорид является электролитом, то есть способен ионизироваться в водном растворе и образовывать ионы магния (Mg2+) и хлорида (Cl-).
Магний хлорид обладает рядом полезных свойств и областей применения. Он широко применяется в медицине, в основном как источник магния при дефиците этого микроэлемента в организме. Препараты на основе магния хлорида также используются для лечения и профилактики некоторых заболеваний нервной системы, таких как неврозы, бессонница и т.д. Кроме того, магний хлорид применяется в косметической промышленности для производства дезодорантов и антиперспирантов, благодаря своей антисептической и антипотное действию.
Таким образом, реакция магния с соляной кислотой приводит к образованию магния хлорида, который обладает свойствами электролита и применяется в различных сферах жизни, начиная от медицины и заканчивая промышленностью. Фундаментальное изучение этой реакции позволяет понять особенности взаимодействия различных веществ и применить эти знания на практике.
Варианты использования полученного продукта
Получаемый продукт реакции магния с соляной кислотой – хлорид магния, является важным химическим соединением, которое может быть использовано в различных областях.
1. Применение в медицине
Хлорид магния широко используется в медицине в форме растворов для инъекций. Он применяется для лечения магниевой недостаточности, снижения кровотока и давления, регулирования сердечной активности, а также для профилактики преждевременных схваток у беременных женщин.
2. Производство фармацевтических препаратов
Хлорид магния является компонентом некоторых фармацевтических препаратов, которые применяются для лечения заболеваний сердца, нервной системы, почек и других патологий. Он используется в качестве смягчающего и противовоспалительного средства.
3. Промышленное использование
Хлорид магния находит применение в ряде промышленных отраслей. Он используется для изготовления магниевых сплавов, которые широко применяются в авиационной и автомобильной промышленности. Также хлорид магния используется в процессе производства фармацевтических, пищевых и косметических продуктов.
4. Бытовое и садоводческое использование
Хлорид магния, благодаря свойствам смягчать воду, может быть использован в бытовом хозяйстве для удаления накипи и вредных примесей из воды. Он также применяется в садоводстве для подкормки растений, так как магний является важным элементом питания для растений.
Эксперименты с магнием и соляной кислотой в научных и технических исследованиях
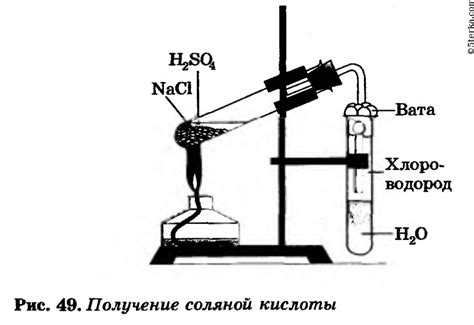
В ходе научных и технических исследований широко используются эксперименты с магнием и соляной кислотой. Магний – это активный металл, который обладает высокой химической реактивностью. Соляная кислота, в свою очередь, является одной из наиболее распространенных кислот в химической лаборатории.
Особенностью реакции магния с соляной кислотой является выделение водорода. При взаимодействии магния с соляной кислотой происходит образование хлорида магния и выделение водорода. Эта реакция сопровождается сильным физическим эффектом – образованием пузырьков газа и его быстрым выходом из реакционной смеси.
Эксперименты с магнием и соляной кислотой применяются в различных областях науки и техники. Например, в химических исследованиях такие эксперименты позволяют изучать химические свойства и реакционную способность магния. В технических исследованиях эксперименты с магнием и соляной кислотой могут быть использованы для производства водорода, который является перспективным источником энергии.
Значительное применение эксперименты с магнием и соляной кислотой находят также в образовательных целях. Школьные и университетские лаборатории проводят подобные эксперименты для демонстрации химических реакций, обучения студентов химии и объяснения основных закономерностей химической превращаемости веществ.
Опасности при проведении реакции и меры предосторожности
Проведение реакции магния с соляной кислотой может представлять опасность для здоровья и безопасности, поэтому необходимо соблюдать определенные меры предосторожности.
Одна из основных опасностей при проведении этой реакции - это выделение взрывоопасного водорода. Возможность возникновения взрыва требует особой осторожности и надлежащего обращения с реагентами.
Перед началом эксперимента необходимо провести химический анализ соляной кислоты на наличие примесей в металлическом оборудовании. С этой целью обычно используют каплю соляной кислоты и каплю аммиака, очень щепетильно следить за тем, чтобы оба флакона, а также инструменты не имели примесей.
Среди мер предосторожности также следует упомянуть необходимость выполнения реакции в хорошо вентилируемом помещении или под вытяжным шкафом, чтобы предотвратить скопление опасных газов в воздухе и обеспечить безопасность оператору.
В случае кожного контакта с соляной кислотой или продуктами реакции необходимо мгновенно промыть зону контакта большим количеством воды и обратиться к врачу, если состояние ухудшается. Следует помнить, что соляная кислота является агрессивным химическим веществом и может вызвать ожоги и другие повреждения кожи и слизистых.
В целях безопасности необходимо также использовать специальную защитную экипировку, такую как химически стойкие перчатки, защитные очки и фартук. Это поможет предотвратить случайный контакт с реагентами и уменьшить риск получения травмы или химического ожога.
Наконец, следует отметить, что проведение данной реакции должно осуществляться только под руководством опытного химика или под контролем квалифицированного преподавателя. Это поможет минимизировать риски и обеспечить безопасность всех участников эксперимента.
Вопрос-ответ
Какая реакция происходит между магнием и соляной кислотой?
Между магнием и соляной кислотой происходит реакция, в результате которой образуется хлорид магния и выделяется водородный газ.
Какие вещества участвуют в реакции магния с соляной кислотой?
В реакции магния с соляной кислотой участвуют магний (Mg) и соляная кислота (HCl).
Что происходит, когда магний реагирует с соляной кислотой?
При реакции магний растворяется в соляной кислоте, образуя хлорид магния (MgCl2) и выделяя водородный газ (H2).
Каковы особенности реакции магния с соляной кислотой?
Особенности реакции магния с соляной кислотой включают выделение водорода, образование хлорида магния и протекание реакции с выделением тепла.
Какие проявления можно наблюдать во время реакции магния с соляной кислотой?
Во время реакции магния с соляной кислотой можно наблюдать выделение пузырьков водорода, появление плавающего магния в растворе и возможное изменение цвета раствора.
Как проводится реакция между магнием и соляной кислотой в лаборатории?
В лаборатории реакцию между магнием и соляной кислотой можно провести, поместив полоску или кусочек магния в колбу с соляной кислотой и наблюдая за выделением водорода и растворением магния.
