Металлы являются одними из основных материалов, используемых в промышленности, строительстве и многих других отраслях жизни. Их широкое применение можно объяснить не только их механическими свойствами, но и особенностями их химической структуры. Одной из наиболее важных характеристик металлов является их твердость.
Твердость металлов обусловлена особым строением их кристаллической решетки. Металлы образуют кристаллы, в которых атомы находятся в упорядоченном состоянии. Они связаны между собой с помощью межатомных связей. Прочность металла определяется силой этих связей. Чем выше сила связей, тем тверже будет металл.
Твердость металлов также зависит от наличия дефектов в кристаллической решетке. Дефекты могут возникать в результате неправильно ориентированных атомов или наличия дополнительных атомов в кристалле. Эти дефекты могут способствовать укреплению кристаллической структуры и повышению твердости металла.
В целом, твердость металлов является результатом сложного взаимодействия между химическими и структурными особенностями. Понимание этих особенностей позволяет разрабатывать новые материалы с определенными свойствами и улучшать существующие.
Таким образом, химия несомненно играет ключевую роль в определении твердости металлов. Изучение химической структуры и взаимодействий внутри металлической матрицы позволяет улучшать свойства металлов и расширять их область применения.
Причина твердости металлов
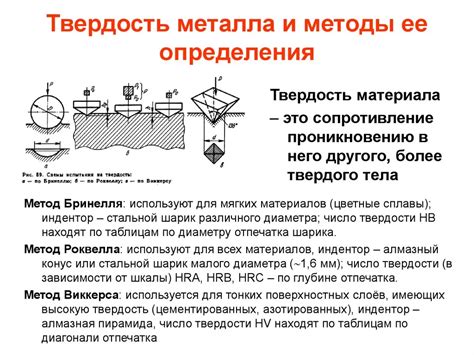
Твердость металлов - это свойство, которое характеризует их способность сопротивляться деформации, изгибу и царапинам. Отличительной особенностью металлов является их кристаллическая структура, которая в значительной степени определяет их твердость.
Металлы обладают высокой твердостью благодаря особому взаимному расположению атомов в их кристаллической решетке. Кристаллическая структура металлов образуется за счет регулярного повторения элементарной ячейки, которая состоит из атомов. Такое упорядочение атомов в кристаллической решетке позволяет металлам сопротивляться деформации и обеспечивает их твердость.
В металлах присутствуют два типа взаимодействий между атомами - ионное и металлическое. Ионное взаимодействие обусловлено наличием заряда у атомов металла, что обеспечивает силу притяжения между ними. Металлическое взаимодействие происходит благодаря образованию электронного облака, которое связывает атомы в металлической решетке. Эти взаимодействия упрочняют кристаллическую структуру металла и придают ему твердость.
Также твердость металлов может быть связана с наличием вторичных фаз или прочных и твердых сплавов. Путем добавления других элементов в металл возможно усиление его структуры и повышение твердости. Например, добавление к углероду железа приводит к образованию сплава стали, который обладает высокой твердостью.
Металлы - химические элементы
Металлы являются одной из главных групп химических элементов и обладают рядом особенностей, отличающих их от других классов веществ. Они обычно имеют блестящую поверхность и хорошо проводят тепло и электричество. Металлы можно обнаружить во множестве природных и искусственных материалов, таких как монеты, провода, автомобили и здания.
Одной из основных характеристик металлов является их способность образовывать ионные соединения. Большинство металлов имеют тенденцию отдавать электроны для образования положительных ионов. Это связано с их строением атома, в котором внешние электроны находятся в так называемой проводимости, что обеспечивает высокую электропроводность у металлов.
Металлы также обладают способностью к формированию кристаллической решетки. Атомы металлов регулярно упорядочены в кристаллических решетках, что придает металлам их характерную структуру и прочность. Наличие регулярной структуры также обусловливает другие важные свойства металлов, такие как пластичность и способность к деформации под воздействием внешних нагрузок.
Структура металлической решетки
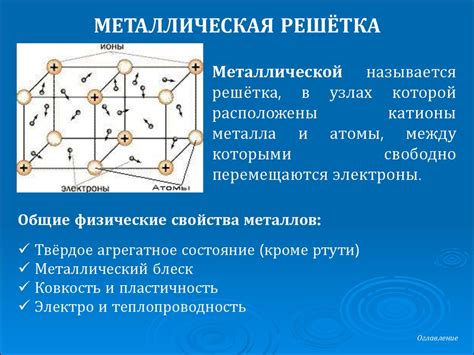
Металлические материалы обладают высокой твердостью благодаря своей специфической структуре. Основной элемент металлической решетки – это кристаллическая решетка. Она образуется в результате упорядоченного расположения атомов или ионов металла.
Металлическая решетка состоит из положительно заряженных ионов металла и свободных электронов. Положительно заряженные ионы являются ядрами атомов металла, а свободные электроны перемещаются между ионами.
Плотность металлической решетки определяется величиной межатомного расстояния и количеством атомов в единице объема. Чем плотнее решетка, тем выше твердость металла. В металлической решетке атомы имеют плотное упакованное расположение и формируют трехмерную сетку.
Свободные электроны в металлической решетке не привязаны к конкретным атомам и свободно перемещаются по всей структуре. Именно они обуславливают основные свойства металлов, такие как электропроводность и теплопроводность.
Одной из причин высокой твердости металлов является связь между атомами иионами металла. Она осуществляется за счет сил притяжения между положительно заряженными ионами и свободными электронами, которые "приклеивают" ионы друг к другу.
Межатомные связи в металлах
Твердость металлов обусловлена особым типом межатомных связей, которые образуются в кристаллической решетке металла. Главными типами межатомных связей в металлах являются металлическая связь и связь атомов за счет ковалентной природы.
Металлическая связь основана на деликатном, но прочном взаимодействии между металлическими атомами. Эта связь образуется благодаря наличию свободных электронов, которые движутся между положительно заряженными ядрами. Такое взаимодействие позволяет атомам быть плотно упакованными в кристаллической решетке и обеспечивает высокую твердость металлов.
Связь атомов в металлах через ковалентные электроны также играет важную роль в обеспечении твердости. Ковалентная связь возникает, когда два атома делят пару электронов, образуя между собой общую электронную облако. Это позволяет атомам металла удерживать друг друга и укреплять структуру металлической решетки.
Таким образом, межатомные связи в металлах обеспечивают прочность и твердость данного материала. Они позволяют металлам выдерживать напряжения и деформации без разрушения, что делает их незаменимыми для множества различных применений в современной индустрии.
Роль электронов в металлической решетке
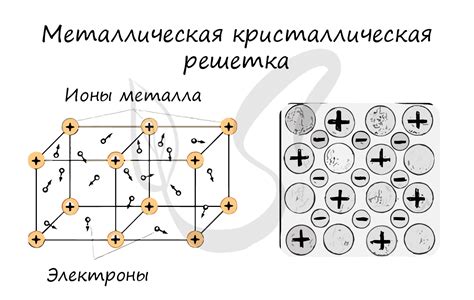
Электроны играют важную роль в формировании твердости металлов. Они обладают низкой массой и отрицательным зарядом, что позволяет им двигаться свободно внутри металлической решетки.
Электроны образуют так называемое электронное облако вокруг атомов металла. Это облако состоит из отдельных электронов, которые совместно с атомными ядрами создают металлическую решетку. Электроны сильно связаны с атомными ядрами, но приложение внешнего воздействия, такого как удар или давление, может нарушить эту связь.
В результате нарушения связи между атомными ядрами и электронами, электроны начинают свободно двигаться по металлической решетке. Их движение создает электрический ток, который вызывает образование поверхностного эффекта.
Поверхностный эффект обусловливает силу связи между атомами и, следовательно, обеспечивает твердость металлов. Чем плотнее и более близко расположены атомы в металлической решетке, тем больше электронов участвует в процессе формирования связей, и тем более твердым является металл.
Электроны также играют роль в проводимости металлов. Их свободное движение позволяет электронам передавать электрический ток внутри металлов. Это объясняет хорошую электропроводность металлов и их способность проводить тепло.
Vзаимодействие металлов с другими элементами
Металлы - это элементы, которые обладают высокой термической и электрической проводимостью. Они также известны своей твердостью и стойкостью к механическим воздействиям. Однако, металлы могут взаимодействовать с другими элементами, что приводит к образованию различных соединений и сплавов.
Взаимодействие металлов с кислородом - один из наиболее распространенных процессов. При контакте металла с кислородом воздуха происходит окисление, что приводит к образованию окисленных соединений. Например, железо при окислении превращается в ржавчину. Окисление металлов может быть предотвращено путем нанесения защитных покрытий, таких как оксиды или лаки.
Металлы также могут реагировать с кислотами. К ним относятся реакции между металлом и солями кислот, которые приводят к образованию солей металлов. Например, при взаимодействии меди с соляной кислотой образуется соль меди(II) хлорида.
Некоторые металлы могут взаимодействовать с водой. Например, щелочные металлы, такие как натрий и калий, быстро реагируют с водой, образуя гидроксиды и выделяя водород. Другие металлы, такие как железо или алюминий, могут реагировать с водой только при наличии катализатора или в при наличии иона водорода.
Также, металлы могут реагировать с другими элементами, такими как сера или фосфор. Реакция металлов с серой приводит к образованию сульфидов металлов, а с фосфором - к образованию фосфидов. Например, алюминий может реагировать с серой, образуя сульфид алюминия. Эти соединения могут иметь различные свойства и применения, например, соединения серы могут использоваться в качестве катализаторов или смазок, а фосфиды могут быть использованы в производстве батарей или полупроводниковых материалов.
Вопрос-ответ
Почему металлы обладают твердостью?
Металлы обладают твердостью из-за особой структуры и связей между атомами. В кристаллической решетке металлов атомы расположены регулярно и между ними есть сильные металлические связи. Эти связи обеспечивают прочность и твердость металлов.
Как металлы получают свою твердость?
Металлы получают свою твердость благодаря специальной обработке, которая меняет их структуру. Например, обжигание, закалка или легирование металлов могут увеличить их твердость. Также, добавление других элементов в металл может повысить его прочность и твердость.
Можно ли изменить твердость металла?
Да, твердость металла можно изменить различными способами. Например, путем закалки или обжигания металла можно увеличить его твердость. Также, добавление легирующих элементов в металл может повысить его прочность и твердость. Однако, в некоторых случаях изменение твердости металла может привести к потере его других полезных свойств.
Какие факторы влияют на твердость металлов?
На твердость металлов влияют различные факторы, включая их химический состав, структуру и обработку. Некоторые металлы, такие как сталь, могут быть более твердыми изначально из-за своего состава. Другие металлы могут быть обработаны специальными методами, чтобы увеличить их твердость. Также, легирование металлов может повысить их твердость и прочность.
Какая роль химии в твердости металлов?
Химия играет важную роль в твердости металлов. Особенности химической структуры металлов, атомные связи и взаимодействия между атомами определяют их твердость. Также, химические процессы, такие как легирование, могут изменять структуру и свойства металлов, включая их твердость.
Можно ли сделать металл мягким?
Да, с помощью определенных методов обработки и изменения структуры металла, его можно сделать мягким. Например, нагревание и последующая быстрая охладка (закалка) металла может уменьшить его твердость и сделать его более пластичным. Также, мягкие металлы могут быть получены путем добавления определенных элементов в металлическую матрицу.
