Взаимодействие концентрированной азотной кислоты (HNO3) с различными металлами является важной темой в области химии. В данной статье рассматривается взаимодействие HNO3 с металлами Mg (магний) и Fe (железо) при низких температурах.
Магний и железо являются важными металлами в промышленности и обладают высокой химической активностью. Исследования показали, что концентрированная азотная кислота взаимодействует с магнием и железом при низких температурах, образуя комплексные соединения.
Одной из особенностей взаимодействия азотной кислоты с магнием и железом при низких температурах является образование нитратов в результате реакции между HNO3 и соответствующим металлом. Нитраты магния и железа имеют широкое применение в различных отраслях промышленности, включая производство удобрений и взрывчатых веществ.
Также в статье представлены результаты экспериментальных исследований, проведенных с использованием различных методов анализа. Было установлено, что взаимодействие HNO3 с магнием и железом при низких температурах происходит медленно, и для полного протекания реакции необходимо повышение температуры.
Исследования взаимодействия концентрированной азотной кислоты с металлами Mg и Fe при низких температурах имеют практическое значение для промышленности и могут быть использованы при разработке новых технологий производства и примененных исследований.
Реакция азотной кислоты с металлами Mg и Fe при низких температурах
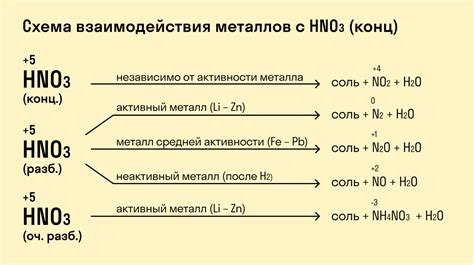
Взаимодействие концентрированной азотной кислоты с металлами Mg и Fe при низких температурах является сложным и неоднозначным процессом.
Азотная кислота (HNO3) считается одним из наиболее активных оксидирующих агентов. При низких температурах она способна интенсивно взаимодействовать с металлами Mg и Fe, образуя соответствующие нитратные соединения.
Реакция азотной кислоты с металлом Мg протекает с выделением газообразного продукта - оксида азота (NO), который хорошо виден благодаря своему характерному красноватому цвету. На поверхности металла Мg образуется пассивирующая (защитная) пленка оксида магния (MgO), которая предотвращает дальнейшее окисление металла.
С другой стороны, взаимодействие азотной кислоты с металлом Fe при низких температурах может вызывать более активное окисление и разрушение поверхности металла. Происходит образование нитрата железа (Fe(NO3)2), который растворяется в кислоте, а на поверхности металла могут образовываться различные окисные продукты.
Изучение реакции азотной кислоты с металлами Mg и Fe при низких температурах является важным для понимания основных принципов окислительно-восстановительных процессов, происходящих в металлах и их соединениях.
Влияние концентрированной азотной кислоты на металл Mg
Концентрированная азотная кислота (HNO3) является сильным окислителем и может оказывать влияние на металлы. Одним из металлов, реагирующих с азотной кислотой, является магний (Mg).
Реакция Mg с азотной кислотой протекает достаточно интенсивно и сопровождается выделением газов, а также образованием пены из диоксида азота и воды. В результате этой реакции образуется нитрат магния (Mg(NO3)2).
При воздействии азотной кислоты на магний могут также наблюдаться окислительные реакции, сопровождающиеся образованием оксида магния (MgO) и выделением нитрилов (R-NO2) и оксидов азота.
Реакция между концентрированной азотной кислотой и магнием является экзотермической, то есть сопровождается выделением тепла и энергии. Это может привести к возгоранию вещества в результате высокотемпературного окисления.
Важно учитывать, что взаимодействие концентрированной азотной кислоты с металлом Mg может привести к образованию опасных веществ, поэтому необходимо соблюдать меры безопасности при работе с этими веществами.
Химическая реакция между азотной кислотой и металлом Fe
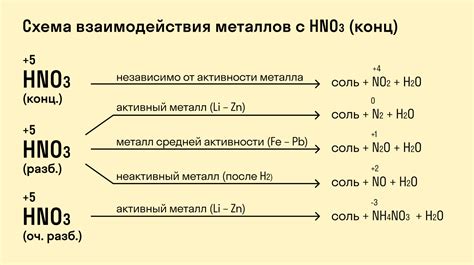
Азотная кислота (HNO₃) относится к сильным окислителям и может взаимодействовать с различными металлами, включая железо (Fe). При этом начинается химическая реакция, в результате которой образуются соответствующие соли и выделяется диоксид азота (NO₂).
Во время взаимодействия азотной кислоты с железом, происходит окисление железа до двухвалентного состояния, образуя ион Fe²⁺. Реакция протекает экзотермически и осуществляется при наличии катализаторов, таких как фосфорная кислота (H₃PO₄) или серная кислота (H₂SO₄).
Химическое уравнение реакции между азотной кислотой и железом можно представить следующим образом:
Fe + 4HNO₃ → Fe(NO₃)₂ + 2H₂O + 2NO₂
Полученная в результате реакции соль, Fe(NO₃)₂, является парамагнитным веществом и может применяться в различных областях, включая химическую промышленность и земледелие.
Важно отметить, что взаимодействие азотной кислоты и железа может протекать с выделением большого количества тепла и газа. Поэтому при обработке азотной кислотой следует соблюдать осторожность и работать в хорошо проветриваемых помещениях или под дымоудаляющими устройствами.
Кинетика взаимодействия азотной кислоты с металлами Mg и Fe
Вводное предисловие: Взаимодействие азотной кислоты с металлами Mg и Fe является одной из важных тем в области химии и материаловедения. Изучение кинетики этого процесса имеет большое значение для понимания механизма реакции и оптимизации условий взаимодействия.
Экспериментальные исследования: Для изучения кинетики взаимодействия азотной кислоты с металлами Mg и Fe проводятся эксперименты при низких температурах. В ходе этих экспериментов измеряются скорость реакции и количество образующихся продуктов. Результаты исследований позволяют определить зависимость скорости реакции от концентрации азотной кислоты и температуры.
Механизм взаимодействия: Изучение кинетики взаимодействия азотной кислоты с металлами Mg и Fe позволяет выявить основные стадии процесса и определить механизм реакции. Обычно вначале происходит адсорбция азотной кислоты на поверхности металла, затем идет диссоциация и реакция с поверхностью. Механизм реакции может быть сложным и варьировать в зависимости от концентрации азотной кислоты и температуры.
Практическое применение: Изучение кинетики взаимодействия азотной кислоты с металлами Mg и Fe имеет важное практическое значение. На основе полученных данных возможно определение оптимальных условий и режимов взаимодействия, которые могут быть использованы при производстве различных материалов и промышленных процессах. Кроме того, полученные результаты могут быть использованы при разработке новых катализаторов и материалов с улучшенными свойствами.
Применение реакции металла с азотной кислотой при низких температурах
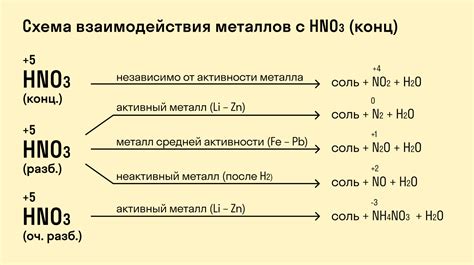
Реакция металла с азотной кислотой при низких температурах является важным процессом в химии и находит применение в различных сферах.
Одним из примеров использования данной реакции является производство удобрений. Металлы, такие как магний и железо, реагируют с азотной кислотой, образуя соединения, которые могут быть использованы в качестве удобрений для растений. Эти соединения содержат азот, который является необходимым элементом для роста и развития растений.
Другим примером применения реакции металла с азотной кислотой является производство взрывчатых веществ. Металлы, такие как магний, реагируют с азотной кислотой при низких температурах, образуя нитраты металла. Нитраты металла могут быть использованы в производстве взрывчатых веществ, таких как тринитротолуол (ТНТ).
Также, реакция металла с азотной кислотой при низких температурах может быть использована в аналитической химии. Данная реакция может помочь определить содержание металлов в различных образцах. Путем анализа образца на образование нитратов металла, можно определить его концентрацию и наличие веществ.
Вопрос-ответ
Как взаимодействует концентрированная азотная кислота с металлом Mg?
Концентрированная азотная кислота реагирует с металлом Mg, образуя соль и выделяя водород. Это реакция окисления металла.
Какой продукт образуется при взаимодействии концентрированной азотной кислоты с металлом Fe?
При взаимодействии концентрированной азотной кислоты с металлом Fe образуется соль и выделяется оксид азота. Это реакция окисления металла.
Почему концентрированная азотная кислота обладает окислительными свойствами?
Концентрированная азотная кислота обладает окислительными свойствами из-за наличия атомов кислорода, способных переходить в более высокую степень окисления при реакции с другими веществами, такими как металлы.
Какая температура считается низкой для взаимодействия концентрированной азотной кислоты с металлами Mg и Fe?
Для взаимодействия концентрированной азотной кислоты с металлами Mg и Fe считается низкой температура около 25 градусов Цельсия.
