Валентность металлов побочных подгрупп является одной из важнейших характеристик элементов, определяющей их химические свойства и способность образования соединений. Валентность определяется количеством электронов, участвующих в химической связи металла с другими атомами. Это свойство может быть изменяемым и зависит от многих факторов, таких как взаимодействие с другими элементами, окружающая среда и физические условия.
Определение валентности металлов побочных подгрупп может проводиться различными методами. Один из них - анализ электронной конфигурации атома металла. Металлы побочных подгрупп обладают специфической электронной конфигурацией, которая определяет их химические свойства и способность к образованию соединений. Например, металлы побочных подгрупп 1 и 2 имеют валентность, соответствующую количеству электронов на внешнем энергетическом уровне (с учетом ионизационных потенциалов), а металлы побочной группы 14 имеют валентность, равную 4.
Еще одним методом определения валентности металлов побочных подгрупп является анализ их окислительно-восстановительных свойств. Металлы побочных подгрупп обладают различной активностью в реакциях окисления и восстановления. Исходя из этого, можно определить валентность металла, основываясь на его реакционной способности.
Таким образом, определение валентности металлов побочных подгрупп является важным шагом в изучении химических свойств элементов. Знание валентности позволяет предсказывать и объяснять химические реакции и свойства соединений, а также прогнозировать способность металла образовывать различные соединения и соединяться с другими элементами.
Определение валентности металлов

Валентность металлов побочных подгрупп может быть определена с помощью различных методов и экспериментов. Одним из таких методов является анализ реакций, которые эти металлы могут проводить с другими веществами.
При изучении валентности металлов побочных подгрупп активно применяется качественный анализ. При этом проводятся различные химические реакции с известными реагентами, а затем анализируется полученная продукция.
Кроме того, валентность металлов побочных подгрупп можно определить исходя из их электронной конфигурации. Для этого необходимо провести расчеты, учитывая количество электронов в различных энергетических оболочках.
Для удобства определения валентности металлов побочных подгрупп существуют таблицы, в которых указаны значения валентностей для каждого металла. При использовании таких таблиц необходимо учитывать, что валентность металла может меняться в зависимости от условий reaksiya-i-vzaimodeystvie-veshchestv/.
Таким образом, определение валентности металлов побочных подгрупп является важной задачей в химии. Это позволяет более точно изучать химические свойства этих металлов и применять их в различных областях науки и промышленности.
Валентность металлов побочных подгрупп
Металлы побочных подгрупп, такие как медь, цинк, свинец, железо и другие, имеют различную валентность в химических соединениях. Валентность металлов определяет, сколько электронов они могут отдать или принять при образовании связей с другими элементами.
Валентность металлов побочных подгрупп зависит от их электронной конфигурации. Например, медь имеет валентность +1 и +2, что соответствует потере одного или двух электронов из внешней электронной оболочки. Цинк обычно имеет валентность +2, так как он теряет два электрона, чтобы достичь стабильной конфигурации.
Однако, валентность металлов побочных подгрупп может быть иная в различных соединениях. Например, железо может иметь валентность +2 или +3 в соединениях, в зависимости от окружающих элементов и условий реакции.
Изучение валентности металлов побочных подгрупп важно для понимания и предсказания их химического поведения. Это помогает в синтезе новых соединений и разработке новых материалов с определенными свойствами.
Методы определения валентности
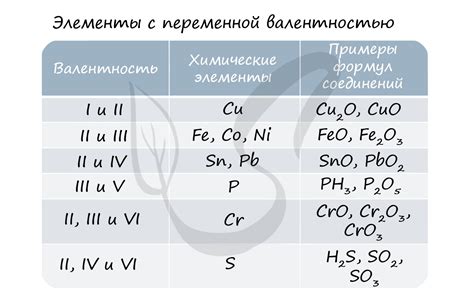
Определение валентности металлов побочных подгрупп является важной задачей в химии. Валентность металла определяет его способность образовывать ионные соединения и вступать в реакции с другими элементами. Существует несколько методов, которые позволяют определить валентность металлов побочных подгрупп.
Один из методов определения валентности это анализ химических реакций. Металлы побочных подгрупп обычно образуют ионы с определенной валентностью при взаимодействии с другими элементами. Изучение реакций металла с кислородом, серой и другими неметаллами позволяет определить его валентность. Если металл образует ионы с разной валентностью, то его валентность можно определить по балансу химических уравнений.
Еще одним методом определения валентности является исследование степени окисления металла в соединении. Степень окисления металла показывает сколько электронов металл отдал или принял при образовании иона. Изучение структуры соединения и анализ электронного строения металла позволяют определить его степень окисления и, соответственно, валентность.
Также для определения валентности металлов побочных подгрупп используется метод измерения электропроводности. Металлы с разной валентностью имеют разную электропроводность. Измерение электропроводности позволяет определить валентность металла, особенно при использовании специальных устройств и методов, таких как измерение электрического сопротивления материала при различных условиях.
Примеры определения валентности
1. Определение валентности по периодической системе
Первый и наиболее простой способ определения валентности металлов побочных подгрупп основывается на периодической системе химических элементов. Валентность металла определяется по номеру его группы в периодической системе. Например, металл из группы 1 имеет валентность 1, из группы 2 – валентность 2.
2. Определение валентности по химическим реакциям
Еще один способ определения валентности металлов побочных подгрупп заключается в анализе их химических реакций. Например, если металл взаимодействует с кислородом и образует оксид, то его валентность равна заряду оксида. Также можно определить валентность металла по его соединениям с другими элементами, учитывая заряды и стехиометрию реакции.
3. Определение валентности по электрохимической активности
Еще один способ определения валентности металлов побочных подгрупп основывается на их электрохимической активности. Металлы с более высокими значениями электрохимического потенциала имеют более высокую валентность. Например, железо (Fe) встречается в двух валентностях: Fe(II) и Fe(III), причем Fe(III) имеет более высокий электрохимический потенциал.
Важность определения валентности

Валентность металлов побочных подгрупп играет важную роль в химических процессах и реакциях, поскольку определяет их способность образовывать соединения с другими элементами. Точное определение валентности металлов побочных подгрупп позволяет установить возможные варианты их соединений и предсказать их свойства.
Знание валентности помогает в определении степени окисления металла, а также его способность к образованию ионов. Так, металлы побочных подгрупп имеют различные степени окисления, что влияет на их химическую активность и способность образовывать соединения с другими элементами.
Определение валентности металлов побочных подгрупп особенно важно при изучении неорганической химии и разработке новых материалов. Зная валентность металла, можно предсказать его взаимодействие с другими элементами и составить более точные химические уравнения.
Валентность также имеет значение в промышленности, где металлы побочных подгрупп используются в процессе производства различных материалов, включая сплавы, катализаторы и электроды. Определение валентности позволяет выбрать правильный металл для конкретной задачи и обеспечить нужные характеристики и свойства готового продукта.
Вопрос-ответ
Как определить валентность металлов побочных подгрупп?
Определить валентность металлов побочных подгрупп можно, исходя из их расположения в таблице Менделеева. Например, металлы 1 группы имеют валентность +1, металлы 2 группы - +2, металлы 13 группы - +3 и т.д. Есть некоторые исключения, но в большинстве случаев эта система дает достаточно точные результаты.
Можно ли определить валентность металлов побочных подгрупп по их внешней электронной оболочке?
Да, валентность металлов побочных подгрупп можно определить по количеству электронов на их внешней электронной оболочке. Например, металлы, у которых на внешней оболочке 1 электрон, имеют валентность +1, металлы с 2 электронами - +2, с 3 электронами - +3 и т.д.
Какие металлы побочных подгрупп имеют валентность +1?
Металлы побочных подгрупп, имеющие валентность +1, включают литий, натрий, калий, рубидий, цезий и франций.
Какие металлы побочных подгрупп имеют валентность +2?
Металлы побочных подгрупп, имеющие валентность +2, включают бериллий, магний, кальций, стронций, барий и радий.
Какие металлы побочных подгрупп имеют валентность +3?
Металлы побочных подгрупп, имеющие валентность +3, включают бор, алюминий, галлий, индий и таллий.
Какие металлы побочных подгрупп имеют валентность +4?
Металлы побочных подгрупп, имеющие валентность +4, включают углерод, кремний, германий, олово и свинец.
Какие металлы побочных подгрупп имеют валентность -3?
Металлы побочных подгрупп, имеющие валентность -3, включают антимон и бисмут.
