HNO3, или азотная кислота, является одним из важных химических соединений, используемых в различных отраслях. Это сильная кислота, которая имеет множество применений, начиная от производства удобрений и пластмасс до использования в лабораториях и фармацевтической промышленности.
С точки зрения химической формулы HNO3, можно сделать вывод, что она состоит из атомов азота (N), кислорода (O) и водорода (H). Отсутствие металлического элемента в формуле говорит о том, что HNO3 является неметаллическим соединением.
Однако, важно отметить, что азотная кислота образуется путем реакции между неметаллом - азотом, источником кислорода и воды. Другими словами, азотная кислота может быть получена только при наличии какого-либо металла в процессе синтеза. Таким образом, азотная кислота является результатом взаимодействия неметалла с металлическим оксидом.
В заключении, можно сказать, что HNO3 является неметаллическим соединением, состоящим из атомов азота, кислорода и водорода. Однако, она образуется путем реакции неметалла - азота с металлическим оксидом, что подтверждает его важное место среди химических соединений, используемых в различных отраслях промышленности и исследований.
Что такое HNO3 и какие свойства у него?

HNO3 - это химическое обозначение для соединения, известного как азотная кислота. Она является одной из самых известных и широко используемых кислот в химии.
Азотная кислота является бесцветной или слегка желтоватой жидкостью, имеющей характерный запах. Она очень коррозийна и может вызвать ожоги на коже и слизистых оболочках.
Свойства азотной кислоты:
- Азотная кислота обладает сильной кислотностью, поэтому она является сильным окислителем.
- Она растворяется легко в воде, образуя концентрированное растворение с пониженным рН. Этот раствор может вызывать ожоги.
- Азотная кислота реагирует с многими металлами и неметаллами. Например, она окисляет металлы, такие как медь и железо, образуя соответствующие соли и оксиды.
- Она используется в производстве удобрений, взрывчатых веществ, пластиков и многих других химических соединений.
Несмотря на свою опасность и коррозионные свойства, азотная кислота - важное вещество в химической промышленности и научных исследованиях из-за своей способности взаимодействовать с различными веществами и проводить окислительные реакции. Она играет важную роль в химических процессах и позволяет получать множество нужных соединений и материалов.
HNO3: кислота ли, оксид металла или неметалла?
HNO3 - это химическое соединение, называемое азотной кислотой. Она является одним из основных оксидов неметалла - азота.
Азотная кислота получается путем растворения оксида азота(IV) NO2 в воде.
Химическая формула азотной кислоты - HNO3, указывает на ее состав: одна молекула воды H2O и одна молекула оксида азота(IV) NO2.
Азотная кислота имеет сильно выраженные кислотные свойства и широко используется в промышленности и лабораторных условиях.
Она при взаимодействии с металлическими и неметаллическими оксидами, образует соли - нитраты, например, калия, натрия и других металлов.
HNO3 в промышленности и быту

HNO3 (азотная кислота) является одним из самых важных и широко используемых химических соединений в промышленности и быту. Она широко применяется во многих отраслях и играет значительную роль в различных процессах.
Одной из главных областей применения HNO3 является производство удобрений. Азотные удобрения, такие как аммиачная селитра и нитрат аммония, получаются путем реакции азотной кислоты с аммиаком. Они являются основным источником азота для растений и играют ключевую роль в сельском хозяйстве.
Кроме того, HNO3 используется в процессе производства взрывчатых веществ, таких как тротил и нитроглицерин. Она служит кислотной компонентой, необходимой для создания стабильных химических соединений, обладающих высокой взрывоопасностью. Без азотной кислоты производство этих веществ было бы невозможным.
В промышленности HNO3 также используется как растворитель и окислитель. Ее высокая реакционная активность позволяет использовать ее в процессах выделения и очистки различных соединений. Кроме того, азотная кислота используется в производстве различных химических продуктов, таких как красители и пластмассы.
В быту азотная кислота широко применяется в качестве чистящего средства. Благодаря своим высоким окислительным свойствам, она позволяет эффективно удалять органические загрязнения и пятна с различных поверхностей. Однако, в связи с ее высокой коррозионной активностью, необходимо соблюдать осторожность при использовании и хранении азотной кислоты в быту.
В заключение, HNO3 является важным химическим соединением, играющим значительную роль в промышленности и быту. Она находит применение в производстве удобрений и взрывчатых веществ, а также используется как окислитель и чистящее средство. Несмотря на свою широкую область применения, взаимодействие с азотной кислотой требует соблюдения осторожности и правил безопасности.
HNO3: едкий или ядовитый?
HNO3, или азотная кислота, известна своим высоким уровнем едкости и острого запаха. На первый взгляд может показаться, что эта кислота является едкой, но на самом деле она также обладает ядовитыми свойствами.
HNO3 сильный окислитель и может вызвать серьезные ожоги кожи, глаз и слизистых оболочек. При попадании на кожу она может вызвать покраснение, жжение и эрозию. Вдыхание паров азотной кислоты может привести к раздражению слизистых оболочек дыхательных путей и легочной пневмонии.
Однако, HNO3 также обладает ядовитым действием. При попадании в организм она может повредить клетки и органы, вызвать отравление и иметь негативный эффект на жизненно важные функции организма. Поступление HNO3 внутрь может вызвать ожоги пищевода и желудка, а также привести к отравлению.
В целом, HNO3 является опасным веществом и требует особой осторожности при использовании. Необходимо соблюдать все меры предосторожности, такие как использование защитной одежды и респиратора, при работе с этой кислотой. При возникновении контакта с кожей или в случае отравления, необходимо немедленно промыть площадь контакта водой и обратиться за медицинской помощью.
Взаимодействие HNO3 с различными веществами
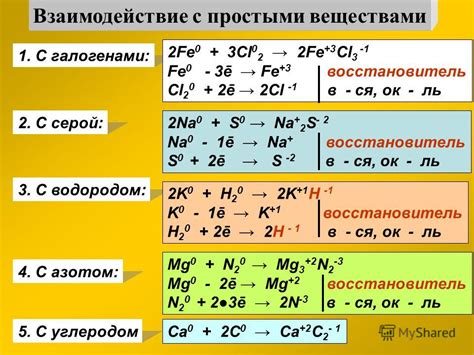
С металлами:
- Вода и HNO3 образуют соль и оксид металла. Например, с медью HNO3 образует нитрат меди (Cu(NO3)2) и диоксид азота (NO2).
- HNO3 взаимодействует с железом, образуя нитрат железа (Fe(NO3)3) и диоксид азота (NO2).
- С цинком HNO3 реагирует, образуя нитрат цинка (Zn(NO3)2) и освобождая диоксид азота (NO2).
С основаниями:
- Взаимодействие HNO3 с гидроксидами оснований приводит к образованию нитратов и воды. Например, с гидроксидом натрия (NaOH) HNO3 образует нитрат натрия (NaNO3) и воду (H2O).
- С аммиаком (NH3) HNO3 реагирует, образуя аммониевый нитрат (NH4NO3) и воду (H2O).
С неметаллами:
- Хлориды, бромиды и иодиды неметаллов образуют хлорноводородную кислоту (HCl), бромноводородную кислоту (HBr) и йодноводородную кислоту (HI) соответственно, когда реагируют с HNO3.
- Сероводород (H2S) и сернистый газ (SO2) также реагируют с HNO3, образуя соответственно нитраты серы и диоксид азота.
С органическими веществами:
- HNO3 способна окислять органические соединения, образуя нитраты и диоксид азота. Например, с этиленом (C2H4) HNO3 реагирует, образуя нитрат этилендиамина (C2H4(NH3)2(NO3)2) и диоксид азота.
- С метаном (CH4) HNO3 реагирует, образуя нитрат метаниловой группы (CH3NO3) и диоксид азота.
HNO3: роль в процессе нитрирования
HNO3 - химическое вещество, известное как азотнокислая кислота или Азотная кислота. Оно является сильным окислительным и нитрирующим агентом.
Роль HNO3 в процессе нитрирования заключается в его способности вступать в реакцию с различными органическими и неорганическими соединениями, осуществляя замещение нитрогруппами. Эта реакция имеет большое промышленное значение и используется для получения различных органических соединений, таких как нитробензол, нитроглицерин и других.
Процесс нитрирования с участием HNO3 может производиться как в присутствии кислоты (бензол + HNO3 + H2SO4), так и без ее участия (например, при нагревании HNO3 и органического соединения).
HNO3 проводит нитрирование как активных ароматических соединений, так и алифатических. Способность к нитрированию зависит от типа углеводорода и наличия активирующих групп. HNO3 способен серьезно изменить свойства соединений, добавив к ним нитрогруппу.
Таким образом, HNO3 является важным агентом в процессе нитрирования, обладающим способностью замещать атомы в соединениях нитрогруппами и получать новые органические и неорганические соединения с разнообразными свойствами и применениями.
Опасности при работе с HNO3

Азотная кислота (HNO3) является сильной кислотой, которая может представлять опасность при неправильном использовании. Эта химическая вещество имеет высокую коррозивную активность и может причинить вред здоровью, если не соблюдаются соответствующие меры предосторожности.
Контакт с кожей или глазами может вызвать ожоги и раздражение. При попадании на кожу, необходимо тщательно промыть затронутую область большим количеством воды и обратиться за медицинской помощью. Если произошло попадание в глаза, необходимо промыть глаза в течение нескольких минут, при этом следует удалять контактные линзы, если они надеты, и незамедлительно обратиться к врачу.
При вдыхании азотной кислоты могут возникнуть проблемы с дыханием, а также респираторные и глазные раздражения. В случае вдыхания азотной кислоты, пострадавшего нужно перевести на свежий воздух и обеспечить покой. Если симптомы ухудшаются, следует обратиться за медицинской помощью.
При использовании азотной кислоты необходимо соблюдать особую осторожность во избежание попадания ее паров в организм через рот или нос. Работа с азотной кислотой должна проводиться в хорошо проветриваемых помещениях или под системой отвода паров и газов.
В целом, осведомленность о рисках и применение соответствующих средств защиты – основные меры, которые необходимо предпринимать для обеспечения безопасной работы с азотной кислотой. Знание правил безопасности и правильного использования азотной кислоты поможет минимизировать риски и обеспечить безопасность при выполнении соответствующих задач.
Вопрос-ответ
Что такое HNO3?
HNO3 - это химическое соединение, которое известно как азотная кислота. Она состоит из элементов азота (N), водорода (H) и кислорода (O).
Можно ли HNO3 назвать оксидом металла?
Нет, HNO3 не является оксидом металла. HNO3 - это кислота, а не оксид. Оксид металла обычно содержит кислород и один или несколько металлических элементов.
Какие свойства имеет HNO3?
HNO3 обладает рядом интересных свойств. Это сильная кислота, которая может реагировать с различными веществами. Она также является окислителем и может нанести вред органическим и неорганическим веществам. Кроме того, HNO3 является коррозивным веществом и может вызывать ожоги на коже и слизистых оболочках.
Какова структура HNO3?
Структура HNO3 состоит из атомов азота, водорода и кислорода. Азотный атом связан с тремя атомами кислорода, а каждый из атомов кислорода связан с атомом водорода. Такая структура обусловливает основные свойства HNO3 - ее кислотность и окислительные свойства.
Какие еще кислоты, кроме HNO3, известны?
В химии известно множество различных кислот. Некоторые из них, помимо HNO3, включают серную (H2SO4), хлороводородную (HCl), азотистую (HNO2) и фосфорную (H3PO4) кислоты. Каждая из них имеет свои уникальные свойства и может быть использована в различных процессах и реакциях.
Может ли HNO3 быть использована в промышленности?
Да, HNO3 широко используется в промышленности. Она может использоваться как кислотное катализатор, окислитель, а также в процессе нитроcellulose и нитроглицерина. HNO3 также используется в производстве удобрений, пластмасс и различных химических соединений.
