Фосфорная кислота (H3PO4) является одним из наиболее распространенных и важных химических соединений. Данная кислота широко используется в различных областях промышленности, таких как производство удобрений, пищевая промышленность, фармацевтика и др. Однако, интересно знать, является ли H3PO4 оксидом металла или неметалла? Ведь оксиды металлов и неметаллов обладают различными свойствами и имеют существенное значение в химии.
Для ответа на данный вопрос необходимо вспомнить основные химические свойства фосфора и кислорода. Фосфор (P) - неметалл, который обладает высокой активностью и имеет склонность образовывать кислоты. Кислород (O) - также неметалл, обладающий сильной окислительной и восстановительной способностью. Из этих двух элементов и образована фосфорная кислота.
Фосфорная кислота является кислотой неорганического происхождения и образуется в результате соединения фосфора с кислородом.
Оксиды: основные понятия

Оксиды – это неорганические соединения, состоящие из металла или неметалла и кислорода. Они являются самыми распространенными соединениями в химии и сыграли важную роль в развитии человеческой цивилизации.
Оксиды обладают различными химическими свойствами и широко применяются в различных отраслях промышленности. Они играют важнейшую роль в процессах окисления и восстановления, а также в химических реакциях с участием воды.
В зависимости от состава оксида, он может быть одноосновным или двухосновным. Одноосновные оксиды состоят из одного элемента и кислорода, например, СО2 (углекислый газ). Двухосновные оксиды содержат два элемента и кислород, например, SO2 (диоксид серы).
Оксиды также делятся на амфотерные и неамфотерные. Амфотерные оксиды способны проявлять свойства как оснований, так и кислот. Например, оксид алюминия Al2O3 может реагировать с кислотами, образуя соли, а также растворяться в щелочах. Неамфотерные оксиды обладают только кислотными или только основными свойствами.
Оксиды играют значимую роль в природе. Например, диоксид углерода CO2 служит дыханием для растений, а оксиды азота участвуют в процессах атмосферной циркуляции. Кроме того, многие оксиды используются в производстве керамики, стекла, металлов и других материалов.
Окислители и восстановители: ключевые различия
Окислители и восстановители – это основные понятия в химии, связанные со сменой окислительного состояния атомов или ионов химического вещества. Окислительные и восстановительные реакции являются основой для понимания механизмов многих химических процессов и реакций.
Окислители – вещества, которые способны взаимодействовать с другими веществами и передавать им кислородные атомы или группы. В результате этой реакции окислитель сам уменьшается, теряя электроны. Окислители способны окислять другие вещества, при этом они сами восстанавливаются.
Восстановители – вещества, которые способны взаимодействовать с другими веществами и передавать им восстановленные электроны. В результате этой реакции восстановитель сам окисляется, получая электроны от окисляемого вещества. Восстановители способны восстанавливать окисляемые вещества, при этом сами окисляются.
Ключевые различия между окислителями и восстановителями:
- Реакция: окислители окисляют другие вещества, а восстановители восстанавливают окисляемые вещества.
- Электронный обмен: окислители получают электроны от окисляемых веществ, восстановители передают электроны окисляемым веществам.
- Изменение окислительного состояния: окислители сами уменьшаются, теряя электроны, восстановители сами окисляются, получая электроны.
- Роль в химической реакции: окислители реагируют с окисляемыми веществами, восстановители передают электроны окисляемым веществам.
Окислители и восстановители играют важную роль в многих химических процессах, включая окислительно-восстановительные реакции, электрохимические и биохимические процессы. Понимание различий между ними позволяет более глубоко изучать и анализировать механизмы и свойства различных химических веществ, а также применять их в практических целях.
H3PO4: что это такое?
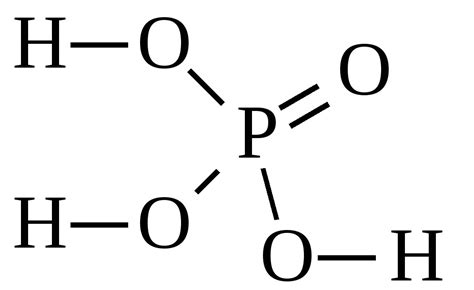
H3PO4 – химическое вещество, которое известно также как ортофосфорная кислота. Это бесцветная жидкость, которая обладает кислым вкусом и характерным запахом. Она является сильной двухосновной (тетропротической) кислотой, которая может отдать три протона.
Ортофосфорная кислота широко применяется в различных отраслях промышленности и науки. Ее основное применение – производство неорганических фосфатных соединений, которые используются в сельском хозяйстве как удобрения. Кроме того, она является основным сырьем при производстве фосфорных солей, фосфорной кислоты натрия и других соединений.
В медицине ортофосфорная кислота применяется как очистительный и антисептический раствор для обработки ран. Она также используется как компонент в составе лекарственных препаратов, позволяющих снизить приступы и желудочные боли при острых заболеваниях.
Ортофосфорную кислоту можно получить как путем химического синтеза, так и из естественных минералов, например, фосфорита. В лаборатории синтезируют ортофосфорную кислоту путем реакции оксида фосфора(V) с водой. Эта реакция сопровождается выделением большого количества теплоты.
В заключение, H3PO4 или ортофосфорная кислота является важным химическим веществом, которое имеет широкий спектр применения в различных отраслях промышленности и медицины. Ее основные свойства, такие как кислотность и растворимость, позволяют использовать ее в процессах производства и для лечебных целей.
Химические свойства H3PO4
Фосфорная кислота (H3PO4) является соединением средней силы, обладающим широким спектром химических свойств. Она проявляет как кислотные, так и окислительные свойства.
В первую очередь, H3PO4 является трехосновной кислотой, которая может отдавать три протона (H+) в реакциях с основаниями. Это позволяет ей образовывать соли, такие как фосфаты, с различными ионами металлов.
Например:
- Фосфорная кислота реагирует с гидроксидом натрия (NaOH) и образует натриевый фосфат (Na3PO4) и воду (H2O).
- H3PO4 отдает протоны оксиду кальция (CaO) и образует кальций фосфат (Ca3(PO4)2).
Кроме того, H3PO4 обладает окислительными свойствами. В реакциях окисления она способна принимать электроны, что позволяет ей окислять другие соединения.
Например:
- Фосфорная кислота окисляет ферросоединения и образует ферри фосфаты (FePO4).
- Она также способна окислять гидроксиды металлов, образуя соответствующие окислы.
Фосфорная кислота также обладает способностью к образованию эфиров с алкоголями, кетонами и другими соединениями. Это позволяет ей использоваться в синтезе органических соединений.
Значительное количество H3PO4 применяется в химической промышленности для производства удобрений, стекла, пищевых добавок и других продуктов. В медицине фосфорная кислота используется для лечения заболеваний почек и некоторых других заболеваний.
H3PO4 и его роль в промышленности

H3PO4, также известная как фосфорная кислота, играет важную роль в промышленных процессах. Фосфорная кислота является оксокисью фосфора, смесью оксидов и кислоты, которая широко используется в различных отраслях промышленности.
Применение в пищевой промышленности:
Фосфорная кислота часто используется в пищевой промышленности как добавка E338. Она используется в процессе консервирования, приготовления напитков и производства пищевых продуктов, таких как газированные напитки, кетчупы, джемы и многие другие продукты. Она также используется в процессе регулирования pH и добавления кислотности в некоторых продуктах.
Применение в химической промышленности:
Фосфорная кислота играет важную роль в химической промышленности. Она используется в процессе производства удобрений, пластмасс, моющих средств, красителей и других химических продуктов. Она также используется в качестве катализатора в различных химических реакциях.
Применение в металлургической промышленности:
Фосфорная кислота играет важную роль в металлургической промышленности. Она используется для удаления окислов и примесей из металлических поверхностей, таких как стальные листы и оборудование. Она также используется в процессе обработки металлов и создания сплавов.
Применение в других отраслях промышленности:
Фосфорная кислота также имеет другие применения в различных отраслях промышленности. Например, она используется в нефтяной промышленности для удаления примесей и осаждения фосфатов. Она также применяется в стекольной промышленности для улучшения свойств стекла. Кроме того, она используется в процессах очистки воды и производстве батарей.
Где можно встретить H3PO4 в природе?
Фосфорная кислота (H3PO4) широко распространена в природе и может быть найдена в различных источниках. Эта кислота очень важна для жизнедеятельности различных организмов и имеет множество применений.
1. В почве: Фосфорная кислота присутствует в почве в виде растворенных солей, которые обеспечивают растения необходимым фосфором для роста и развития. Фосфор является одним из основных макроэлементов, необходимых для фотосинтеза и образования ДНК и РНК.
2. В морской воде: Океаны и моря также содержат фосфорную кислоту в растворенном виде. Эта кислота играет важную роль в цикле фосфора в морской экосистеме и является важным питательным компонентом для водорослей и других морских организмов.
3. В растительных и животных организмах: Фосфорная кислота присутствует в живых организмах в виде фосфатов, которые выполняют различные функции. Например, фосфаты играют важную роль в обмене веществ, энергетическом обмене, структурном образовании костей и зубов, а также в передаче генетической информации.
4. В пищевых продуктах: Фосфорная кислота используется в пищевой промышленности для приготовления различных продуктов, таких как безалкогольные напитки, сыры, молочные продукты и мясные изделия. Она также присутствует в некоторых пищевых добавках, таких как кетчуп, майонез и газированные напитки, чтобы придать им кислый вкус и усилить сохраняемость.
5. В фармацевтической промышленности: Фосфорная кислота используется для производства различных лекарственных препаратов. Она может быть включена в состав антацидов, препаратов для лечения заболеваний почек и некоторых препаратов для лечения растений.
Все эти и другие источники позволяют получать фосфорную кислоту для различных областей применения и характеризуют ее как важное соединение в природе.
Вопрос-ответ
Что такое H3PO4?
H3PO4 представляет собой химическое соединение, известное как фосфорная кислота.
Является ли H3PO4 оксидом металла или неметалла?
H3PO4 является оксидом неметалла. Фосфор, который является основным компонентом в этом соединении, является неметаллом.
Какой элемент входит в состав H3PO4?
В состав H3PO4 входят элементы водород, фосфор и кислород.
Какие свойства имеет H3PO4?
H3PO4 обладает рядом свойств: он является кислотой и может реагировать с основаниями, аминокислотами и металлами; также он обладает коррозионными свойствами и может растворять металлы. Кроме того, фосфорная кислота обладает мощным окислительным действием.
Зачем используется H3PO4?
H3PO4 используется в различных областях: в химической промышленности для производства удобрений, пищевой промышленности для регулирования кислотности пищевых продуктов, в фармацевтике, для производства моющих средств и др.
Какова структура H3PO4?
Структура H3PO4 состоит из трех атомов водорода, одного атома фосфора и четырех атомов кислорода. Водородные атомы связаны с кислородными, атому фосфора, образуя молекулярную формулу H3PO4.
Можно ли H3PO4 использовать в пищевой промышленности?
Да, H3PO4 используется в пищевой промышленности в качестве регулятора кислотности. Соединение имеет E-номер E338 и разрешено к использованию в пищевых продуктах и напитках в определенных концентрациях.

